钢铁“发蓝”是将钢铁制品浸到某些氧化性的溶液中,在钢铁的表面形成一层四氧化三铁的技术过程。其中一种办法是将钢铁制品浸到亚硝酸钠和浓氢氧化钠的混合溶液中加热到130℃反应。其过程可以用如下化学方程式表示:
① 3Fe + NaNO2 + 5NaOH = 3Na2FeO2 + H2O + NH3↑;
② Na2FeO2 + NaNO2 + H2O -- Na2Fe2O4 + NH3↑ + NaOH (未配平);
③ Na2FeO2 + Na2Fe2O4 + 2H2O = Fe3O4 + 4NaOH;
下列说法不正确的是( )
| A.碱性条件下,NaNO2的氧化性比Na2FeO2、Na2Fe2O4都强 |
| B.反应 ①、②、③ 均是氧化还原反应 |
| C.反应 ② 配平后,H2O的化学计量数是5 |
| D.整个反应过程中每有16.8g Fe参加反应转移0.8mol电子 |
某烃的一种同分异构体只能生成一种一氯代物,该烃的分子式可能为
| A.C3H8 | B.C4H10 | C.C5H12 | D.C6H14 |
下列说法不正确的是
A.将pH=4的某酸稀释10倍,测得其pH<5,则该酸为弱酸
B.相同 pH的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH) < c(Na2CO3)<c(CH3COONa)
C.0.1 mol·L-1的NaHA溶液pH=5,则溶液中:c(HA-)>c(H+)>c(A2-)>c(H2A)
D.向NH4HSO4溶液中滴加NaOH溶液至中性,所得混合液:c(Na+)> c(NH4+)>c(SO42-)>c(OH-)
某新型电池NaBH4(B的化合价为+3价)和H2O2作原料,该电池可用作深水勘探等无空气环境电源,其工作原理如下图所示。
下列说法正确的是
| A.电池工作时Na+从b极区移向a极区 |
| B.b极上的电极反应为:H2O2+2e-+2H+=2H2O |
| C.每消耗3molH2O2,转移3mole- |
| D.a极上的电极反应为:BH4-+8OH-+8e-=BO2-+6H2O |
下列叙述正确的是
| A.NaOH浓溶液中滴加FeCl3饱和溶液可制得Fe(OH)3胶体 |
| B.CH3COONa溶液中滴加少量浓盐酸后c(CH3COO-)增大 |
| C.25℃时Fe(OH)3在水中的溶解度大于其在FeCl3溶液中的溶解度 |
| D.SiO2与水反应可制得H2SiO3 |
对于可逆反应:A2(g)+3B2(g)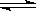 2AB3(g)(正反应放热),下列图象中正确的是
2AB3(g)(正反应放热),下列图象中正确的是