下列依据热化学方程式得出的结论正确的是( )
| A.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=-57.3 kJ·mol-1, 则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3 kJ的热量 |
| B.已知2H2(g)+O2(g)=2H2O(g) △H=-483.6 kJ·mol--1,则氢气的燃烧热为 241.8 kJ·mol-1 |
| C.已知2C(s)+2O2(g)=2CO2(g) △H=a、2C(s)+O2(g)=2CO(g) △H=b, 则a>b |
| D.已知P (白磷,s)=P (红磷,s) △H<0,则红磷比白磷稳定 |
下列说法正确的是
| A.将25g CuSO4·5H2O溶于1L水中,可配制成0.1 mol·L-1CuSO4溶液 |
| B.往FeCl3溶液中滴入KI淀粉溶液,溶液变蓝色 |
| C.用向下排空气法收集NH3,并用湿润的蓝色石蕊试纸检验NH3,是否收集满了 |
| D.向紫色石蕊试液中加入过量的Na2O2粉末,振荡,溶液变为蓝色并有气泡产生 |
物质发生化学变化时,反应前后肯定不发生变化的是
①电子总数 ②原子总数 ③质子总数 ④物质的总质量
⑤物质的总能量 ⑥物质的种类
| A.①②③④⑤ | B.①②③④ | C.②⑤⑥ | D.③④⑤⑥ |
下列物质存 放方法错误的是
放方法错误的是
| A.浓硝酸存放在棕色试剂瓶里 |
| B.FeSO4溶液存放在加有少量铁粉的试剂瓶中 |
| C.碳酸钠溶液盛放在带磨口玻璃塞的细口瓶中 |
| D.金属钠存放于煤油中 |
下列离子方程式书写正确的是
A.硫酸铝溶液中滴加过量浓氨水:Al3+ + 4OH- = AlO + 2H2O + 2H2O |
B.NaHCO3溶液水解:HCO + H2O = H2CO3 + OH- + H2O = H2CO3 + OH- |
C.浓氢氧化钠溶液吸收少量SO2气体:SO2+ 2OH- = SO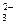 + H2O + H2O |
D.向小苏打溶液中加入醋酸溶液:HCO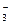 + H+ = CO2↑+ H2O + H+ = CO2↑+ H2O |
金属及其化合物生产和日常生活中有着重要应用。下列有关金属及其化合物的说法不正确的是
A.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 |
B.目前我国流通的硬币是由合金材料制造的 |
C.MgO的熔点很高,可用于制作耐高温材料 |
D.生铁、普通钢和不锈钢中的碳含量依次增加 |