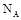 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为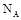 |
B.标准状况下,22.4L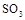 与水反应生成1mol硫酸 与水反应生成1mol硫酸 |
C.足量铜与1L 18mol 浓硫酸反应可以得到 浓硫酸反应可以得到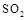 的分子总数为9 的分子总数为9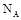 |
D.标准状况下,22.4L任意比的氢气与氧气的混合气体中含有的分子总数均为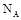 |
在一定温度下,下列叙述不是可逆反应 达到平衡的标志的是:
达到平衡的标志的是:
(1)C的生成速率与C的分解速率相等;
(2)单位时间内a mol A生成,同时生成3a mol B;
(3)A、B、C的浓度不再变化;
(4)混合气体的总压强不再变化;
(5)混合气体的物质的量不再变化;
(6)单位时间消耗amol A,同时生成3amol B;
(7)A 、B、C的分子数目比为1:3:2。
A、(2)(4)(5)
B、(2)(7)
C、(1)(3)(4)
D、(5)(6)(7)
现有可逆反应A(g)+2B(g) n C(g)(正反应放热),在相同温度、不同压强时,A的转化率跟反应时间(t)的关系如图所示,其中结论正确的是
n C(g)(正反应放热),在相同温度、不同压强时,A的转化率跟反应时间(t)的关系如图所示,其中结论正确的是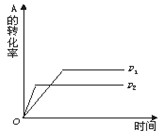
| A.p1> p2, n>3 | B.p1>p2,n=3 |
| C.p1 < p2, n<3 | D.p1<p2,n>3 |
在容积不变的密闭容器中,发生CO(g)+NO2(g) CO2(g)+NO(g)ΔH <0的反应,达到平衡后,降低温度,混合气体的颜色
CO2(g)+NO(g)ΔH <0的反应,达到平衡后,降低温度,混合气体的颜色
| A.变深 | B.变浅 | C.不变 | D.无法判断 |
在新制的氯水中存在平衡:Cl2+H2O HCl+HClO。加入少量下列物质能使c(HClO)增大
HCl+HClO。加入少量下列物质能使c(HClO)增大
| A.CaCO3 | B.NaOH | C.CaSO4 | D.HCl |
一定温度下将1 mol CO和1 mol水蒸气在密闭容器中反应:CO(g)+H2O(g) CO2(g) +H2(g),平衡后测得CO2为0.6mol,再通入4mol水蒸气,达新平衡后CO2的物质的量可能是
CO2(g) +H2(g),平衡后测得CO2为0.6mol,再通入4mol水蒸气,达新平衡后CO2的物质的量可能是
| A.1.2mol | B.1mol | C.0.8mol | D.0.6mol |