“封管实验”具有简易、方便、节约、绿色等优点,观察下列四个“封管实验”(夹持装置未画出),判断下列说法正确的是( )
A.加热时,a上部聚焦了 ,说明 ,说明 的热稳定性比较好 的热稳定性比较好 |
B.加热时,发现b中 变为紫色蒸气,在上部又聚焦为紫黑色固体 变为紫色蒸气,在上部又聚焦为紫黑色固体 |
| C.加热时,c中溶液红色变深,冷却后又逐渐变浅 |
| D.水浴时,d内气体颜色变浅,e内气体颜色变深 |
氢氧化镁在水中存在下列平衡:Mg(OH)2(固)≒ Mg2+ + 2OH-,加入下列物质可使Mg(OH)2固体减少的是()
| A.碳酸钠 | B.硫酸镁 |
| C.硝酸铵 | D.氢氧化钠 |
在一定温度下,可逆反应A(g)+3B(g)≒2C(g)达到平衡的标志是()
A. C的生成速率与C的分解速率相等
B. 单位时间生成nmolA,同时生成3nmolB
C. A、B、C的浓度不再变化
D. A、B、C的分子数比为1:3:2
一定条件下,向一带活塞的密闭容器中充入1 mol N2和3mol H2,发生下列反应:N2(g)+3H2(g)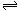 2NH3(g),反应达到平衡后,改变下述条件,NH3气体平衡浓度不改变的是()
2NH3(g),反应达到平衡后,改变下述条件,NH3气体平衡浓度不改变的是()
| A.保持温度和容器压强不变,充入1 mol NH3(g) |
| B.保持温度和容器体积不变,充入1 mol NH3(g) |
| C.保持温度和容器压强不变,充入1 mol N2(g) |
| D.保持温度和容器体积不变,充入1 mol Ar(g) |
E. 保持温度和容器体积不变,充入1 mol H2(g)
把Ca(OH)2固体放入一定量的蒸馏水中,一定温度下达到平衡:
Ca(OH)2(s)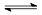 Ca2+(aq)+2OH-(aq)。当向悬浊液中加少量生石灰后,若温度保持不变,下列判断正确的是()
Ca2+(aq)+2OH-(aq)。当向悬浊液中加少量生石灰后,若温度保持不变,下列判断正确的是()
| A.溶液中Ca2+数目减少 | B.溶液中c(Ca2+)增大 |
| C.溶液pH值不变 | D.溶液pH值增大 |
如图所示,图中a曲线表示X(g) +Y(g)≒2Z(g)+ W(s)+ Q的反应过程,若使a曲线变为b曲线,可采取的措施是()
| A.加入催化剂 |
| B.增大Y的浓度 |
| C.降低温度 |
| D.增大体系压强 |
