某学生的实验报告所列出的下列数据中合理的是
| A.用10mL量筒量取7.13mL稀盐酸 |
| B.用托盘天平称量25.20g NaCl |
| C.用广泛pH试纸测得某溶液的pH为2.3 |
| D.用25mL滴定管做中和滴定时,用去某浓度的碱溶液21.70mL |
下列叙述正确的是( )
| A.金属钠、镁等活泼金属着火时,可以使用泡沫灭火器来灭火 |
| B.称取等质量的两份铝粉,分别加入过量的稀盐酸和过量的NaOH溶液,充分反应后,放出氢气的体积(同温同压下)相等 |
| C.向NaHCO3溶液中滴入Ba(OH)2溶液无沉淀,而向Na2CO3溶液中滴入Ba(OH)2溶液出现白色沉淀 |
D.某无色溶液中加Ba(NO3)2溶液,再加入稀盐酸,产生白色沉淀,则原溶液中一定含有SO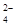 |
下列叙述正确的是( )
| A.同一元素不可能既表现金属性,又表现非金属性 |
| B.氯化氢溶于水能导电,但液态氯化氢不能导电 |
C.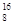 O、 O、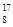 O和 O和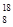 O互为同位素,均属于氧元素,且性质完全相同 O互为同位素,均属于氧元素,且性质完全相同 |
| D.导电性强的溶液里自由移动的离子数目一定比导电性弱的溶液里自由移动的离子数目多 |
下列有关颜色的变化与氧化还原反应无关的是( )
| A.浓硝酸在光照下颜色会变黄 |
| B.在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后溶液的红色褪去 |
| C.向滴有酚酞的NaOH溶液中通入Cl2,溶液褪色 |
| D.向FeSO4溶液中滴加NaOH溶液,生成的沉淀由白色变成灰绿色,最后变成红褐色 |
联合国气候变化大会于2009年1 2月7日~18日在丹麦首都哥本哈根召开,焦点议题之一是发展“低碳经济”,减少温室气体排放。你认为下列做法中,不能有效减少空气中CO2含量的是( )
| A.开发利用太阳能、风能、生物能、海洋能等清洁能源 |
| B.使用节能产品,推广节能环保汽车 |
| C.植树造林,增加森林植被面积 |
| D.用脱硫处理的煤代替原煤作燃料 |
如图所示,锥形瓶内盛有干燥的气体X,胶头滴管内盛有液体Y,若挤压胶头滴管,使液体Y滴入瓶中,振荡,一会儿可见小气球a鼓起。则气体X和液体Y不可能的是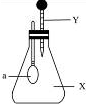
| A.X是Cl2,Y是NaOH溶液 |
| B.X是HCl,Y是NaCl的稀溶液 |
| C.X是SO2,Y是NaOH溶液 |
| D.X是CO2,Y是稀硫酸 |