氧化还原反应中实际上包含氧化和还原两个过程。某氧化还原反应的一个还原过程的反应式为:S2O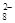 +2e-
+2e- 2SO
2SO ,该反应中另一重要反应物可能是KMnO4、Na2CO3、MnSO4、KNO3四种物质中的一种。下列有关说法正确的是( )
,该反应中另一重要反应物可能是KMnO4、Na2CO3、MnSO4、KNO3四种物质中的一种。下列有关说法正确的是( )
A.S2O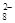 中S显+7价,说明S的最外层有7个电子 中S显+7价,说明S的最外层有7个电子 |
| B.该反应中另一重要反应物为KMnO4 |
C.该反应的氧化过程可表示为:Mn2+-5e-+4H2O MnO MnO +8H+ +8H+ |
D.若有5mol S2O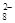 参与反应,溶液中会生成8 mol H+ 参与反应,溶液中会生成8 mol H+ |
“类推”是一种常用的学习方法,但有时会产生错误的结论,下列类推结论中正确的是
| A.IVA族元素氢化物熔点顺序是:GeH4>SiH4>CH4;则VA族元素氢化物熔点顺序也是:AsH3>PH3>NH3 |
| B.第二周期元素氢化物的稳定性顺序是:HF>H2O>NH3;则第三周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3 |
| C.工业上用电解氯化镁制备镁单质,工业上也可用电解氯化铝制备铝单质 |
| D.Fe3O4可改写成氧化物的形式为:FeO·Fe2O3 ;因此Pb3O4也可改写为:PbO·Pb2O3 |
下列离子方程式中正确的是
| A.小苏打溶液中滴加足量石灰水:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O |
| B.向NH4Al(SO4) 2溶液中滴入Ba(OH)2恰好使SO42-反应完全: 2Ba2++4OH-+Al3++2SO42-=2BaSO4↓+AlO2-+2H2O |
| C.次氯酸钠溶液中通入SO2气体:2ClO-+SO2+H2O=2HClO+SO32- |
| D.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:2Fe2++2H++H2O2=2Fe3++2H2O |
下列各组单质中,前者在一定的条件下能将后者从其化合物中置换出来的是
①Al、Fe②Cl2、S③Mg、C④H2、Cu⑤C、Si
A.只有①③ B.只有②④ C.①②③④ D.①②③④⑤
下列与化学反应能量变化相关的叙述正确的是
| A.反应热就是反应放出的热量 |
| B.放热反应的反应速率总是大于吸热反应的反应速率 |
| C.应用盖斯定律,可计算某些难以直接测量的反应热 |
D.同温同压下, 在光照和点燃条件下的 在光照和点燃条件下的 不同 不同 |
下列关于只含非金属元素的化合物的说法中,正确的是
| A.一定是共价化合物 | B.其晶体有可能是离子晶体 |
| C.其晶体不可能是分子晶体 | D.其晶体不可能是原子晶体 |