新型微生物原料电池可以将富含有机物的污水变成干净的水,同时提供电能。该电池中用质子交换膜将正负极分开。工作时,将污水注入反应槽中,污水中的有机物在微生物作用下分解放出电子和质子,质子通过交换膜到另一极与富含氧气的水反应。下列说法正确的是
| A.注入污水的一极是电池的负极,发生氧化反应 |
| B.注入污水的一极是电池的正极,发生氧化反应 |
| C.这种新型微生物燃料电池适宜处理硫酸厂的废水 |
| D.用葡萄糖表示污水中的有机物,通入污水一极的电极反应为 |
C6H12O6+6O2 6CO2+6H2O
6CO2+6H2O
下列实验过程中产生的现象与右边座标图形相符合的是
| A.稀盐酸滴加到一定量NaOH溶液中 (横坐标是稀盐酸的体积,纵坐标为钠离子物质的量) |
| B.铁粉加到一定量CuSO4溶液中 (横坐标是铁粉的质量,纵坐标为沉淀质量) |
| C.CO2通入一定量NaOH溶液中 (横坐标是CO2的体积,纵坐标为溶液的导电能力) |
| D.稀硫酸滴加到Ba(OH)2溶液中 |
(横坐标是稀硫酸的体积,纵坐标为溶液的导电能力)
FeC13、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是
| A.溶液中一定不含Cu2+ | B.溶液中一定含Fe2+ |
| C.加入KSCN溶液一定不变红色 | D.剩余固体中可能含有Fe |
对于某些常见离子的检验及结论一定正确的是
| A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- |
| B.加入氯化钡溶液有白色沉淀产生,再加盐酸沉淀不消失,一定有SO42- |
| C.加入氯化钠溶液有白色沉淀产生,再加稀硝酸沉淀不消失,一定有Ag+ |
| D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
下列离子方程式的书写正确的是
| A.金属铁溶于盐酸中:2Fe+6H+=2Fe3++3H2↑ |
| B.实验室用大理石和稀盐酸制取CO2:2H++CO32-= CO2↑+H2O |
| C.向AlCl3溶液中加入过量的氨水:Al3++3OH-= Al(OH)3↓ |
D.MnO2固体和浓盐酸反应制氯气:MnO2+4H++2Cl- Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O |
下图是一种试验某气体化学性质的实验装置,图中B为开关。若先打开B,在A处通入干燥的氯气,C中红色布条颜色无变化;当关闭B在A处通入干燥的氯气时,C中红色布条颜色褪去。则D瓶中盛有的溶液是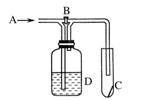
| A.浓硫酸 | B.饱和NaCl溶液 |
| C.浓NaOH溶液 | D.浓NaI溶液 |