下列离子方程式中,正确的是( )
| A.稀硫酸与NaOH溶液反应2H++OH-=H2O |
| B.AgNO3溶液与NaCl溶液反应 Ag++Cl-=AgCl↓ |
| C.CaCO3与稀盐酸反应 CO32-+2H+=CO2↑+H2O |
| D.Fe片插入FeCl3溶液中 Fe+Fe3+=2Fe2+ |
一定条件下,在体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:2X(g)+Y(g)  Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是
Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是
| A.达到平衡时X浓度为0.04 mol/L |
| B.将容器体积变为20 L,Z的平衡浓度变为0.015mol/L |
| C.若增大压强,平衡向正方向移动,平衡常数变大 |
| D.若升高温度,X的体积分数增大,则该反应的DH>0 |
合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g)  2NH3(g),ΔH<0,673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是
2NH3(g),ΔH<0,673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是
| A.点a的n(H2)和点b的n(NH3)比值为3:2 |
| B.点 c处反应达到平衡 |
| C.点d (t1时刻) 和点 e (t2时刻) 处n(N2)不一样 |
| D.其他条件不变,773K下反应至t1时刻,n(H2)比上图中d点的值大 |
通常人们把拆开1mol某化学键吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以估计化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。下表是一些化学键的键能。
| 化学键 |
C—H |
C—F |
H—F |
F—F |
| 键能/(kJ·mol-1) |
414 |
489 |
565 |
155 |
根据键能数据估算下列反应CH4(g)+4F2(g)===CF4(g)+4HF(g)的反应热ΔH为
A.-1940kJ·mol-1 B.1940kJ·mol-1C.-485kJ·mol-1 D.485kJ·mol-1
右图为反应2SO2+O2 2SO3的速率v(SO2)变化的图像,则横坐标可能是
2SO3的速率v(SO2)变化的图像,则横坐标可能是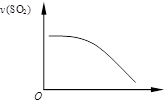
| A.反应时间 | B.温度 |
| C.压强 | D.SO2的浓度 |
爱迪生电池在充电和放电时发生的反应:Fe+NiO2+2H2O Fe(OH)2+Ni(OH)2,下列对该蓄电池推断错误的是:
Fe(OH)2+Ni(OH)2,下列对该蓄电池推断错误的是:
①放电时,Fe参与负极反应,NiO2参与正极反应
②充电时,阴极上的电极反应式为:Fe(OH)2 + 2e-=" Fe" + 2OH-
③放电时,电解质溶液中的阴离子向正极方向移动
④放电时,负极上的电极反应式为:Fe + 2H2O-2e- = Fe(OH)2 + 2H+
⑤蓄电池的电极必须浸入某种碱性电解质溶液中
| A.只有③ | B.③④ | C.④⑤ | D.①②⑤ |