下列说法中正确的是( )
| A.需加热才能发生的反应一定是吸热反应 |
| B.任何放热反应在常温条件一定能发生反应 |
| C.反应物和生成物分别具有的总能量决定了反应是放热反应还是吸热反应 |
| D.ΔH的大小与热化学方程式的计量系数无关 |
分别放置在下图所示装置(都盛有0.1 mol·L-1的H2SO4溶液)中的四个相同的纯锌片,腐蚀最慢的是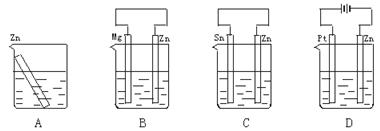
用石墨作电极电解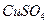 溶液。通电一段时间后(电解质未用完),欲使电解液恢复到起始状态,应向溶液中加入适量的
溶液。通电一段时间后(电解质未用完),欲使电解液恢复到起始状态,应向溶液中加入适量的
A.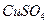 |
B.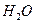 |
C.CuO | D.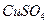 ·5 ·5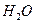 |
在铁制品上镀一定厚度的锌层,以下方案设计合理的是
| A.锌做阳极,铁制品做阴极,溶液中含有锌离子 |
| B.铂作阴极,铁制品做阳极,溶液中含有锌离子 |
| C.铁做阳极,铁制品做阴极,溶液中含有亚铁离子 |
| D.锌做阴极,铁制品做阳极,溶液中含有锌离子 |
铅蓄电池的工作原理为: 研读下图,下列判断不正确的是
研读下图,下列判断不正确的是
A.K 闭合时,d电极反应式 |
B.当电路中转移0.2mol电子时,I中消耗的 为0.2 mol 为0.2 mol |
C.K闭合时,II中 向c电极迁移 向c电极迁移 |
| D.K闭合一段时间后,II可单独作为原电池,d电极为正极 |
电子计算机所用钮扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应是: Zn + 2OH- -2e-="=ZnO" + H2O Ag2O +H2O + 2e-="=2Ag" +2 OH-,下列判断正确的是
| A.锌为正极,Ag2O为负极 | B.锌为负极,Ag2O为正极 |
| C.原电池工作时,正极区溶液pH减小 | D.原电池工作时,负极区溶液pH增大 |