已知0.1mol/L的醋酸溶液中存在电离平衡:CH3COOH 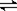 CH3COO-+H+。要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是
CH3COO-+H+。要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是
| A.加少量烧碱溶液 | B.降低温度 |
| C.加少量冰醋酸 | D.加水 |
可以用来鉴别乙烷和乙烯的方法是
| A.用足量的NaOH溶液 | B.用溴的CCl4溶液 |
| C.在光照条件下与Cl2反应 | D.在Ni催化、加热条件下通入H2 |
下列属于同分异构体的是
| A.CH4和CH3CH3 |
| B.CH3-CH2-Cl和CH2Cl-CH2Cl |
| C.CH2=CHCH2CH3和CH3CH=CHCH3 |
D. |
在乙醇CH3CH2OH中化学键如图,则下列说法中正确的是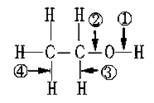
| A.当该醇发生催化氧化时,被破坏的键是②③ |
| B.当该醇与Na反应时,被破坏的键是① |
| C.当该醇与羧酸发生酯化反应时,被破坏的键是② |
| D.当该醇发生消去反应时,被破坏的键是①和④ |
下列醇既能被催化氧化生成醛,又能发生消去反应生成烯烃的是
| A.CH3OH | B.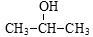 |
C. |
D.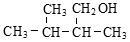 |
普伐他汀是一种调节血脂的药物,其结构简式如图所示(未表示出其空间构型)。下列关于普伐他汀的描述正确的是
| A.分子中含有3种官能团 |
| B.可发生加成反应、氧化反应 |
| C.在水溶液中羧基和羟基均能电离出H+ |
| D.1 mol该物质最多可与l molNaOH反应 |