难挥发性二硫化钽(TaS2)可采用如图所示的装置提纯。将不纯的TaS2粉末装入石英管一端,抽成真空后引入适量的碘并封管,置于加热炉中。反应如下:
TaS2 (s)+2I2 (g)  TaI4 (g)+S2 (g)
TaI4 (g)+S2 (g) 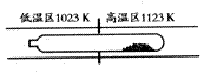
下列说法正确的是( )
| A.在不同温度区域,TaI4 的量保持不变 |
| B.在提纯过程中,I2 的量不断减少 |
| C.在提纯过程中,I2 的作用是将TaS2 从高温区转移到低温区 |
| D.该反应的平衡常数与TaI4 和S2 的浓度乘积成反比 |
某可逆反应过程能量变化如图所示,下列说法中正确的是()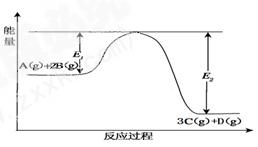

在一瓶PH=1的无色溶液中,已检验出含有Ba 、Ag
、Ag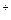 ,则下列粒子:①Cl
,则下列粒子:①Cl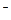 、②Mg
、②Mg 、③Cu
、③Cu 、④ NO
、④ NO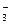 、⑤AlO2—、⑥ CO
、⑤AlO2—、⑥ CO 、⑦NH3·H2O在此溶液中不能大量存在的正确组合是
、⑦NH3·H2O在此溶液中不能大量存在的正确组合是
| A.①②③⑥⑦ | B.②③⑤⑥⑦ | C.①③⑤⑥⑦ | D.①②⑤⑥⑦ |
下列实验能达到目的的是
| 实验 |
 |
 |
 |
 |
| 目的 |
证明铁生锈过程 中空气参与反应 |
证明非金属性 Cl>C>Si |
制取BaSO3, 并吸收尾气 |
从碘水中 分离出碘 |
| 选项 |
A |
B |
C |
D |
化学与能源、环境、生产、生活关系密切,下列说法中不正确的是
| A.环保快餐饭盒的材料可用“玉米塑料”(主要成分为聚乳酸)制成 |
| B.缺铁性贫血在我国居民中普遍存在,可在酱油中添加三价铁盐予以改善 |
| C.松花蛋是一种常用食品,但食用时有氨的气味,可以蘸些食醋除去 |
| D.世博停车场安装催化光解设施,可将汽车尾气中CO和NOx转化为无毒气体 |
在蒸发发皿中加热蒸干并灼烧(低于400℃)下列的溶液,可以得到该物质的固体是
| A.氯化镁铝溶液 | B.硫酸亚铁溶液 | C.碳酸氢钠溶液 | D.硫酸铝溶液 |