人类生活离不开金属。
(1)铁是生活中常用的金属。图6是某“取暖片”外包装的图片。该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热 。
①发热剂需接触到空气才会发热,原因是铁要与 、 等物质共同作用才会生锈。
②推测发热剂成分中氯化钠的作用是 。
(2)应用金属活动性顺序能帮助我们进一步学习金属性质。已知下列各组物质间均能发生置换反应。
A.Fe 和CuSO4溶液 B.Mg和MnSO4溶液 C.Mn和FeSO4溶液
①写出Fe 和CuSO4溶液反应的化学方程式 。
②Mn、Fe、Mg 、Cu四种金属的活动性由强到弱的顺序 。
实验室用如图装置测定空气中氧气含量,在一端封闭的粗玻璃管内放足量白磷,用胶塞塞住,并推入到玻璃管中部,记下位置。置于900C的开水上方加热白磷,白磷燃烧,现象是,胶塞向移动,待装置冷却,胶塞逐渐向移动,最后停留在刻度为处,根据该实验得出的结论是:。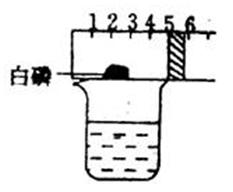
根据质量守恒定律,某化学反应为:2XY+Y2===2Z,则Z的化学式为。
我们研究水的组成时,看到电源两极都由气泡产生,在电源正级的气体验证方法是,电源正负极气体的体积比是。
奥运会田径比赛场上发令枪响后我们看到升起一股白烟,请你写出产生白烟的化学方程式:,其反应基本类型是。
做物质在氧气中燃烧实验时常常在集气瓶中盛少量水或细沙,如:做硫在氧气中燃烧时盛少量水的作用是,做铁丝在氧气中燃烧时盛少量水的作用是。