对溶液中的离子进行鉴定,下列实验所得结论不合理的是
| A.加入稀硝酸后,再加入AgNO3溶液,有白色沉淀生成,则说明原溶液中含有Cl- |
| B.加入KSCN溶液无红色出现,再加入氯水溶液变血红色,说明原溶液中一定含有Fe2+ |
| C.加入用稀硝酸酸化的Ba(NO3)2溶液产生白色沉淀,则可推断原溶液中一定含有SO42- |
| D.加入盐酸产生使澄清石灰水变浑浊的无色无味的气体,可推测原溶液中含有CO32-离子或HCO3- |
我国前科学院院长卢嘉锡与法裔加拿大科学家Gignere巧妙地利用尿素 (H2NCONH2)和H2O2形成加合物H2NCONH2·H2O2,不但使H2O2稳定下来,而且结构也没有发生改变,得到了可供做衍射实验的单晶体,经测定H2O2结构如 图所示,结合以上信息,下列说法不正确的是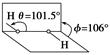
| A.任何分子式中的“· ”都表示氢键 |
| B.H2O2是极性分子,其结构简式为HO—OH |
| C.H2O2既有氧化性又有还原性 |
| D.H2NCONH2与H2O2是通过氢键结合的 |
据权威刊物报道,1996年科学家在宇宙中发现H3分子。甲、乙、丙、丁四位学生对此报道的认识正确的是
| A.甲认为上述发现绝对不可能,因为H3分子违背了共价键理论 |
| B.乙认为宇宙中还可能存在另一种氢单质,因为氢元素有三种同位素必然有三种同素异形体 |
| C.丁认为如果上述的发现存在,则证明传统的价键理论有一定的局限性有待继续发展 |
| D.丙认为H3分子实质上是H2分子与H+以特殊共价键结合的产物,应写成H3+ |
已知磷酸分子的结构如右图所示,分子中的三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不再能跟D2O发生氢交换。由此可推断出 、H3PO2的分子结构是
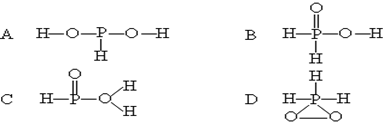
下列有关化学键与晶体结构的说法中,正确的是
| A.含有阴离子的化合物中一定含有阳离子 |
| B.非金属元素组成的化合物一定是共价化合物 |
| C.干冰升华时,分子内共价键会发生断裂 |
| D.两种元素组成的分子中一定只有极性键 |
下列推论正确的是
| A.SiH4的沸点高于CH4,可推测PH3的沸点高于NH3 |
| B.NH为正四面体结构,可推测PH也为正四面体结构 |
| C.CO2晶体是分子晶体,可推测SiO2晶体也是分子晶体 |
| D.C2H6是碳链为直线形的非极性分子,可推测C3H8也是碳链为直线形的非极性分子 |