对某酸性溶液(可能含有Br-,SO42-,H2SO3,NH4+)分别进行如下实验:
①加热时放出的气体可以使品红溶液褪色
②加碱调至碱性后,加热时放出的气体可以使润湿的红色石蕊试纸变蓝;
③加入氯水和四氯化碳时,下层显橙色,再加入BaCl2溶液时,产生的白色沉淀不溶于稀硝酸
对于下列物质不能确认其在溶液中是否存在的是
A Br- B SO42- C H2SO3 D NH4+
下面是4位同学对“化学与健康”这一话题发表的见解中,正确的是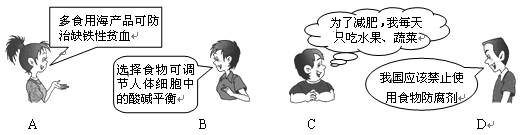
已知CuSO4溶液分别与Na2CO3溶液、Na2S溶液的反应情况如下:
(1)CuSO4 +Na2CO3主要:Cu2+ + CO32─ + H2O ="=" Cu(OH)2↓+ CO2↑
次要:Cu2+ + CO32─="=" CuCO3↓
(2)CuSO4 + Na2S主要:Cu2+ + S2─="=" CuS↓
次要:Cu2+ + S2─+ 2H2O ="=" Cu(OH)2↓+ H2S↑
下列几种物质的溶解度大小的比较中,正确的是
| A.CuS <Cu(OH)2<CuCO3 | B.CuS >Cu(OH)2>CuCO3 |
| C.Cu(OH)2>CuCO3>CuS | D.Cu(OH)2<CuCO3<CuS |
下列叙述不正确的是
A.常温下醋酸分子可能存在于pH>7的碱性溶液中
B.10 mL 0.02 mol·L-1 HCl溶液与10 mL 0.02 mol·L-1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12
C.0.1mol·L-1的氯化铵溶液与0.05mol·L-1的氢氧化钠溶液等体积混合后,混合溶液中离子浓度:c(Cl-)>c(NH4+)>c(Na+)>c(OH-)
D.0.1 mol·L-1某二元弱酸强碱盐NaHA溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H2A)
常温时,将VlmLC1mol·L-1的氨水滴加到V2mLC2mol·L-1的盐酸中,下述结论中正确的是
| A.若混合溶液的pH=7,则C1V1>C2V2 |
| B.若Vl=V2,C1=C2则混合液中c(NH4+)=c(Cl-) |
| C.若混合液的pH=7,则混合液中c(NH4+)>c(Cl-) |
| D.若V1=V2,且混合液的pH<7,则—定有C1<C2 |
常温,某溶液中由水电离产生的c(H+)、c(OH-)满足c(H+)·c(OH—)=10—24,则下列各组离子在该溶液中一定可以大量共存的是
| A.K+、Na+、AlO2—、Cl— | B.Na+、Cl—、SO42—、HCO3— |
| C.NH4+、Na+、NO3—、SO42— | D.Ba2+、Na+、Cl—、NO3— |