用可溶性钡盐检验SO42-离子的存在时,先在待测溶液中加入盐酸,其作用是( )
| A.形成较多的白色沉淀 | B.形成的沉淀纯度更高 |
| C.排除SO42-以外的其它阴离子及Ag+的干扰 | D.排除Ba2+以外的其它阳离子的干扰 |
常温下,向100 mL 0.01 mol·L-1HA溶液中逐滴加入0.02 mol·L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中不正确的是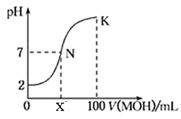
| A.HA一定为一元强酸 |
| B.若x>50,则MOH为一元弱碱 |
| C.N点溶液中:c(A-)=c(M+)>c(OH—)=c(H+) |
| D.若K点对应的溶液的pH=12,则K点溶液中水的电离程度大于0.01 mol·L-1HA溶液中水的电离程度 |
如图所示的电化学装置,下列叙述正确的是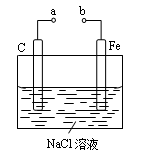
| A.a和b用导线连接,溶液中的Na+向铁电极移动 |
| B.a和b用导线连接,碳电极的电极反应为:O2+2H2O-4e-=4OH— |
| C.a、b分别连接直流电源正、负极,可以防止铁被腐蚀,属于牺牲阳极的阴极保护法 |
| D.若碳电极换成铜电极,氯化钠换成硫酸铜,a、b分别连接直流电源负、正极,可实现铁上镀铜 |
设NA为阿伏伽德罗常数的数值。下列说法正确的是
| A.78g苯中C—C和C=C的个数均是3NA |
| B.标准状况下,NA个SO3分子的体积约是22.4L |
| C.Na与氧气化合生成0.1molNa2O2转移0.4NA个电子 |
| D.常温下,1L 0.1mol·L—1的Na2S溶液中的阴离子数目大于0.1NA |
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是
| 选项 |
叙述Ⅰ |
叙述Ⅱ |
| A |
SO2有弱氧化性 |
SO2能使品红溶液褪色 |
| B |
SiO2能与氢氧化钠、氢氟酸反应 |
SiO2是酸性氧化物 |
| C |
碳酸钠能与酸反应 |
碳酸钠可作治疗胃酸过多的一种药剂 |
| D |
Ksp(CuS)、Ksp(HgS)均很小 |
可用Na2S除去废水中的Cu2+和Hg2+ |
25℃时,下列各组离子在指定溶液中能大量共存的是
| A.在弱碱性溶液中:Na+、K+、Cl-、HCO3- |
B. 的溶液中:Na+、Al3+、SO42-、NO3- 的溶液中:Na+、Al3+、SO42-、NO3- |
| C.与镁反应生成氢气的溶液中:Na+、Fe2+、NO3-、Cl- |
| D.在苯酚溶液中:Fe3+、NH4+、Br-、SO42- |