下列离子方程式正确的是
| A.硫酸氢铵和氢氧化钠等物质的量混合:NH4++OH-=NH3↑+H2O |
| B.碳酸氢钙与过量氢氧化钙溶液反应:Ca2++HCO3-+2OH-=CaCO3↓+2H2O |
| C.Ca(ClO)2溶液中通人SO2气体:Ca2++ClO—+ SO2 +H2O = CaSO3↓+2HClO |
| D.氯气与氢氧化钠溶液反应:Cl2+2OH-=Cl-+ClO-+H2O |
【改编】下列物质的系统命名中,错误的是
| A.CH3—CHBr—CHBr—CH3 2,3-二溴丁烷 |
B.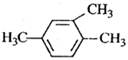 1,3,4-三甲基苯 1,3,4-三甲基苯 |
C.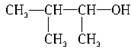 3-甲基-2-丁醇 3-甲基-2-丁醇 |
D.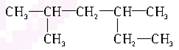 2,4-二甲基己烷 2,4-二甲基己烷 |
下列有机物中,只含有一种官能团的是
| A.氯乙烯 | B.苯 | C.甲苯 | D.乙炔 |
下列说法正确的是
| A.乙烷和乙醇都属烃类化合物 |
| B.有机化合物一定含有碳元素 |
| C.丙烷和丁烷都有同分异构体 |
| D.含有碳元素的化合物一定是有机化合物 |
如图所示是Zn和Cu形成的原电池,其实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是

| A.①②③ | B.②④ | C.④⑤⑥ | D.③④⑤ |
下列说法正确的是
| A.需要加热方能发生的反应一定是吸热反应 |
| B.放热反应在常温下一定很容易发生 |
| C.反应是放热还是吸热,必须看反应物和生成物所具有的总能量的相对大小 |
| D.化学反应只生成新物质,没有能量的变化 |