下列说法正确的是
| A.可逆反应的特征是正反应速率和逆反应速率相等 |
| B.在其他条件不变时,使用催化剂只能改变反应速率,而不能改变化学平衡状态 |
| C.在其他条件不变时,升高温度可以使平衡向放热反应方向移动 |
| D.在其他条件不变时,增大压强一定会破坏气体反应的平衡状态 |
下列物质中不含共价键的是( )
| A.NaCl | B.Cl2 | C.HCl | D.NaOH |
随着人们对事物认识的不断发展,废电池集中进行处理在某些地方得到实施,其首要目的是( )
| A.防止电池中汞、镉、铅等重金属离子污染土壤和水源 |
| B.充分利用电池外壳的金属 |
| C.回收电池中的石墨电极 |
| D.不使电池中渗出的电解质溶液腐蚀其他物品 |
同种元素的不同微粒,它们的( )
| A.电子层数相同 | B.质子数不一定相同 |
| C.相对原子质量一定相同 | D.化学性质一定相同 |
已知元素的质子数,可以推知原子的:①原子序数②核电荷数③离子所带的电荷数④核外电子数,其中正确的是()
| A.①②③ | B.②③ | C.①② | D.①②④ |
下列关于原子的几种描述中,不正确的是()
A.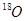 与 与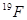 具有相同的中子数 具有相同的中子数 |
B.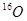 与 与 具有相同的电子数 具有相同的电子数 |
C. 与 与 具有相同的质量数 具有相同的质量数 |
D. 与 与 具有相同的质子数 具有相同的质子数 |