下列各组离子能在指定溶液中大量共存的是
①无色溶液中:Al3+、Cl-、Na+、HCO3-、SO42-
②pH=11的溶液中:Na+、AlO2-、NO3-、S2-、SO32-
③加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、K+、SO42-
④使pH试纸呈红色的溶液中:Fe3+、MnO4-、Na+、SO42-
⑤酸性溶液中:Fe2+、Al3+、NO3-、I-
| A.①②④ | B.①⑤ | C.②③④ | D.①②③ |
用NA表示阿伏加德罗常数,下列说法正确的是
| A.500mL2mol/L葡萄糖溶液中所含分子数为NA |
| B.0.1mol/L Na2CO3溶液中的阴离子总数大于0.1NA |
| C.电解精炼铜时,若阳极质量减少64g,则外电路导线上不一定通过2NA个电子 |
| D.5.6g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA |
能用如图气体制取装置制取少量气体并能“随开随用、随关随停”的是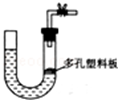
| A.大理石和稀硫酸制取二氧化碳 |
| B.锌粒和稀硫酸制氢气 |
| C.浓盐酸和二氧化锰制取氯气 |
| D.过氧化钠和水制取氧气 |
化学与社会、生活密切相关,下列说法不正确的是
| A.在食品袋中放入盛有CaO和硫酸亚铁的透气小袋,可防止食物受潮、氧化变质 |
| B.MgO、Al2O3的熔点很高,工业上用于制作耐高温材料,也用与冶炼铝和镁 |
| C.发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔 |
| D.利用ClO2对自来水消毒主要是因为ClO2具有强氧化性 |
一定条件下存在反应C(s)+H2O(g)  CO(g)+H2(g):向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示。下列说法正确的是
CO(g)+H2(g):向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示。下列说法正确的是
| 容器 |
甲 |
乙 |
丙 |
| 容积 |
0.5 L |
0.5 L |
V |
| 温度 |
T1 ℃ |
T2 ℃ |
T1 ℃ |
| 起始量 |
2 molC 1 molH2O |
1 molCO 1 molH2 |
4 molC 2 molH2O |

A.甲容器中,反应在前15 min的平均速率v(H2)=0.1 mol·L-1·min-1
B.丙容器的体积V>0.5L
C.当温度为T1 ℃时,反应的平衡常数K=2.25
D.乙容器中,若平衡时n(H2O)=0.4 mol,则T1< T2