设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.标准状况下,189D2O中所含的质子数为10NA |
| B.28gN2和C0的混合气体中含有的分子数为NA |
| C.标准状况下,11.2LO2参加反应转移的电子数一定为2 NA |
| D.5.6g铁与足量稀硫酸反应失去电子数为0.3 NA |
化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是( )
A.CO2的电子式: |
B.S原子的结构示意图: |
C.NH3的结构式为: |
D.质量数为37的氯原子: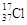 |
设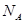 表示阿伏加德罗常数,则下列叙述正确的是
表示阿伏加德罗常数,则下列叙述正确的是
A.标准状况下,22.4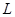 四氯化碳含有 四氯化碳含有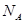 个四氯化碳分子 个四氯化碳分子 |
B.在18gH218O中含有10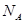 个中子 个中子 |
C.在2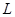 0.5 0.5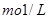 的醋酸溶液中含有 的醋酸溶液中含有 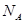 个 个 离子 离子 |
D.常温下,16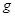 甲烷含有10 甲烷含有10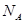 个电子 个电子 |
已知反应AsO43-+2I-+2H+ AsO33-+I2+H2O是可逆反应。设计如图装置(C1、C2均为石墨电极),分别进行下述操作。
AsO33-+I2+H2O是可逆反应。设计如图装置(C1、C2均为石墨电极),分别进行下述操作。
Ⅰ.向B烧杯中逐滴加入浓盐酸
Ⅱ.向B烧杯中逐滴加入40% NaOH溶液
结果发现电流计指针均发生偏转.据此,下列判断正确的是()
| A.操作Ⅰ过程中,C1为正极 |
| B.操作Ⅱ过程中,盐桥中的K+移向B烧杯溶液 |
| C.Ⅰ操作过程中,C2棒上发生的反应为:AsO43-+2H++2e-=AsO33-+H2O |
| D.Ⅱ操作过程中,C1棒上发生的反应为:2I――2e-=I2 |
1913年德国化学家哈伯发明了以低成本制造大量氨的方法,从而大大满足了当时日益增长的人口对粮食的需求。下列是哈伯法的流程图,其中为提高原料转化率而采取的措施是( )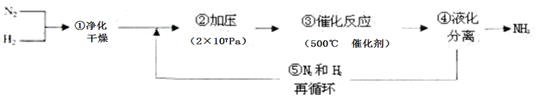
| A.①②③ | B.②④⑤ | C.①③⑤ | D.②③④ |
投入一定量的物质A和B发生可逆反应:2A(g)+nB(g) 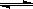 mC(g) ,在温度分别为T1、T2,压强分别为P1、P2的条件下,测得C的物质的量与时间的关系如右图所示, 有关该反应的说法正确的是( )
mC(g) ,在温度分别为T1、T2,压强分别为P1、P2的条件下,测得C的物质的量与时间的关系如右图所示, 有关该反应的说法正确的是( )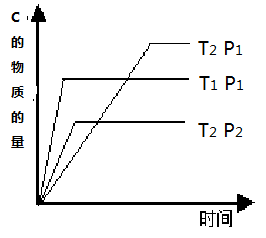
| A.n+2<m该反应正反应为放热反应 |
| B.n+2<m该反应正反应为吸热反应 |
| C.n+2>m该反应正反应为放热反应 |
| D.n+2>m该反应正反应为吸热反应 |