(10,娄底24)配制溶质质量分数一定的氯化钠溶液常按以下操作顺序进行。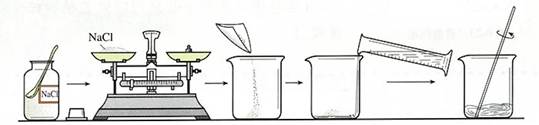
请回答下列问题:
(1)计算配制100g溶质质量分数为5%的氯化钠溶液所需:
氯化钠 40 g,水 41 g。
(2)用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应 42 。
A.增加适量氯化钠固体 B.减少适量氯化钠固体 C.调节平衡螺母
(3)将氯化钠和水依次倒入烧杯中,用玻璃棒搅拌,其目的是 43 。
通过一学期的学习,我们知道了化学是一门以________为基础的学科,实验室操作一定要规范,取用药品要严格按照规定,如果没有说明用量,就应该取最少量,即液体用____mL,固体只要盖满_____。
我市叶县盛产食盐。食盐的主要成分NaCl由离子和离子构成;电解食盐水制烧碱:2NaCl +2H2O 2NaOH+ Cl2↑+X↑,则X的化学式为。
2NaOH+ Cl2↑+X↑,则X的化学式为。
在实验室中,配制500g0.9%的生理盐水:
(1)该实验必备的仪器有托盘天平、药匙、胶头滴管、量筒、细口瓶、烧杯和;
(2)该实验的主要步骤有计算、、溶解、装瓶并贴标签;
水是生命之源。认识水资源、合理利用和保护水资源是我们义不容辞的责任。
(1)生活中常用的方法降低水的硬度。
(2)生活中你是如何节约用水和防止水体污染的(请各举一例)。
节约用水;防止水体污染。
联合国决定2011年为“国际化学年”,其活动主题为“化学——我们的生活,我们的未来”。
(1)化学——使生活丰富多彩。下列主要由有机合成材料制成的是(填序号,下同);
A.涤纶制成的航天服 B.纯棉内衣 C.不锈钢茶杯 D.塑料桶
(2)化学——为健康保驾护航。小超的奶奶骨质疏松,医生建议奶奶使用;
A.葡萄糖酸锌口服液 B.钙片 C.加铁酱油 D.含氟牙膏
(3)化学——让未来充满希望。纳米材料石墨烯可能帮助科学家实现修建太空天梯的构想,石墨烯由碳原子构成,请推测石墨烯可能具有的一条化学性质。