已知25℃,AgI饱和溶液中,C(Ag+)=1.22×10-8mol/L,AgCl饱和溶液中,
C(Ag+)=1.25×10-5mol/L,若在5ml含有KCl和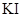 各为0.01mol/L的溶液中加入8mL0.01mol/L的AgNO3溶液,这时溶液中所含溶质的离子浓度大小关系正确的是
各为0.01mol/L的溶液中加入8mL0.01mol/L的AgNO3溶液,这时溶液中所含溶质的离子浓度大小关系正确的是
| A.C(K+)>C(NO3-)>C(Cl-)>C(Ag+)>C(I-) |
| B.C(K+)>C(NO3-)>C(Ag+)> (Cl-)>(I-) |
| C.C(NO3-)>(K+)> C(Ag+)> (Cl-)>(I-) |
| D.(K+)> C(NO3-)>C(Ag+)=(Cl-)+(I-) |
下列叙述正确的是
| A.在氧化还原反应中,金属单质一般只作还原剂 |
| B.氧化还原反应中非金属单质一定是氧化剂 |
| C.金属元素被还原时所得产物一定是金属单质 |
| D.某元素从化合态变为游离态,该元素一定被还原 |
下列物质组合中,既能和盐酸反应又能和烧碱溶液反应的化合物是
①Al②Al2O3 ③Al(OH)3 ④NaHCO3
| A.①②③④ | B.②③④ | C.①③④ | D.①②④ |
合金是一类用途广泛的金属材料,下列物质中不属于合金的是
| A.钢 | B.青铜 | C.黄铜 | D.水银 |
市售的食品包装中常带有一小包铁粉,并标有“吸氧剂”字样,这是利用了铁粉的
| A.氧化性 | B.还原性 | C.吸水性 | D.导电性 |
用NA表示阿伏加德罗常数的值,下列说法中正确的是
| A.1 mol N2所含有的原子数为NA |
| B.标准状况下,22.4 L水中含有的水分子数为NA |
| C.标准状况下,22.4 L氯化氢所含的原子数为NA |
| D.24 g O2和24 g O3所含的氧原子数都是1.5NA |