烯烃A在一定条件下可以按下面的框图进行反应。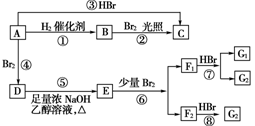
F1和F2互为同分异构体,G1和G2互为同分异构体,D是CCH3BrH3CCCH3BrCH3。
已知1,3-丁二烯与少量溴水加成时有以下两种方式:
CH2CHCHCH2+Br2―→CH2BrCHBrCHCH2(1,2-加成)
CH2CHCHCH2+Br2―→CH2BrCHCHCH2Br(1,4-加成)
试回答下列问题:
(1)A的结构简式为_________________________________________________________。
(2)框图中属于取代反应的是(填数字代号)______________________________________。
(3)框图中①、③、⑥属于________反应。
(4)G1的结构简式为_________________________________________________________。
化合物A经过下列反应后得到一种六元环状酯G。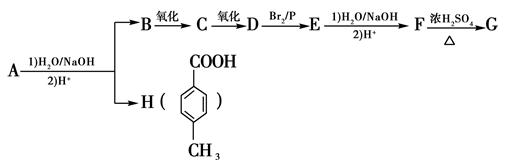
已知F的分子式是C4H8O3,F的核磁共振氢谱显示共有三个峰。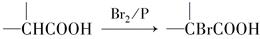
请回答下列问题:
(1) A、B的结构简式分别为、。
(2) 写出F→G反应的化学方程式:。
(3)写出满足下列条件的H的一种同分异构体的结构简式:。
①是苯的对位二取代物;②不能与FeCl3溶液发生显色反应;③不考虑烯醇 (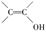 )结构。
)结构。
(4)在G的粗产物中,经检测含有聚合物杂质。写出聚合物杂质可能的结构简式(仅要求写出1种):,形成该聚合物的反应类型为:。
普伐他汀是一种调节血脂的药物,其结构简式如图所示(未表示出空间构型)。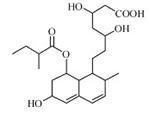
试填空:
(1)该有机物分子中的含氧官能团是。(填名称)
(2)该有机物的分子式为。
(3)该有机物能发生反应。(请填序号)
a.取代反应 b.消去反应 c.加成反应
(4)1 mol该有机物与足量的氢氧化钠溶液充分反应,需要消耗氢氧化钠mol。
下图所示的是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质和反应条件被略去。常温常压下,化合物A是家庭生活中常用的一种调味品,A、C的焰色反应都呈黄色,8是无色无味的液体,D是黄绿色气体,E、F都是无色气体,F的水溶液是盐酸,H的水溶液具有漂白、杀菌性,J在水溶液中生成时为红褐色沉淀。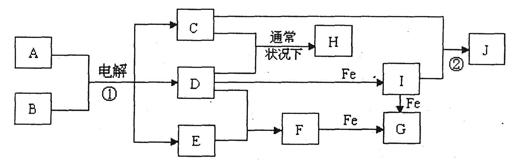
(1)H的化学式为。
(2)F的电子式为。
(3)反应①的化学方程式为。
(4)反应②的离子方程式为。
某无色透明溶液中可能存在大量Ag+、Mg2+、K+、Cu2+中的一种或几种,请填写下列空白。
(1)不用做任何实验就可以肯定溶液中不存在的离子是________________。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是________,反应的离子方程式为_______________。
(3)取(2)的滤液加过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定有________,有关反应的离子方程式为________________。
(4)原溶液中可能大量存在的阴离子是
| A.Cl- | B.NO3- | C.CO3 2- | D.OH- |
氮是生命的基础,由于存在着氮的循环,生命世界才能像我们所见到的那样生机勃勃,充满活力。下图是自然界中氮的循环图,请回答有关问题。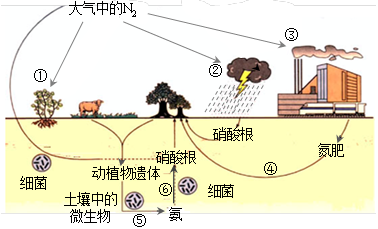
(1)从空气中获取氮是人类长久以来追求的目标。下列有关说法正确的是_________(填序号)。
a.图中①②③④⑤都属于自然界的固氮过程
b.在过程⑥中,氮元素的化合价降低
c.反应②的化学方程式是N2 +O2 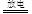 2NO
2NO
d.德国化学家哈伯发明了合成氨工艺,其主要反应如下2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
(2)氨经氧化后可得到硝酸,而硝酸能与氨形成含氮量很高的肥料NH4NO3,施用于土壤而实现非自然形式的氮循环。但这种肥料不适宜与碱性物质共用,否则会降低肥效,其原因是_________________________________(用离子方程式表示)。
(3)人类活动对氮循环产生着明显的影响。汽车尾气中的NO,是造成光化学烟雾的物质之一,但NO对人体又起着独特的生理作用,被誉为“明星分子”,有三位科学家因此项研究成果而获得1998年诺贝尔奖。上述事实说明我们应辨证地看待化学物质的作用。科技人员已经找到了一些解决NO排放的方法。在汽车尾气排放管中安装一个催化转化器,可将尾气中另一种有害气体CO跟NO反应转化为空气中的两种成分。气体在催化剂表面吸附与解吸作用的机理如下图所示。
写出上述变化中的总化学反应方程式____________________________________。