氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于阴影部分的是( )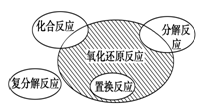
| A.4Fe(OH)2+O2+2H2O===4Fe(OH)3 |
| B.2NaHCO3Na2CO3+H2O+CO2↑ |
| C.2Na2O2+2CO2===2Na2CO3+O2 |
| D.Cl2+2KBr===Br2+2KCl |
下列有关实验装置进行的相应实验,能达到实验目的的是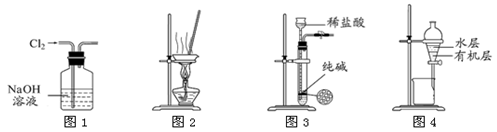
| A.用图1所示装置除去Cl2中含有的少量HCl |
| B.用图2所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
| C.用图3所示装置制取少量纯净的CO2气体 |
| D.用图4所示装置分离CCl4萃取碘水后已分层的有机层和水层 |
下列有关物质性质的应用错误的是
| A.H2O2溶液有氧化性,可用于杀菌消毒 |
| B.氯化镁是一种电解质,可用于电解法制镁 |
| C.液氨汽化时要吸收大量的热,可用作制冷剂 |
| D.Na2SO4能使蛋白质发生变性,可用于提纯蛋白质 |
【改编】常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.pH=12的溶液:NH4+、K+、SO42-、NO3- |
| B.澄清透明的溶液:Mg2+、Na+、SO42-、Br- |
| C.0.1 mol·L-1 Na2CO3溶液:NH4+、Ca2+、SO42-、NO3- |
| D.c(Fe3+)=0.1 mol·L-1溶液:H+、K+、Cl-、SCN- |
【原创】下列有关化学用语表示正确的是
A.核内有8个中子的碳原子: |
B.甲烷分子的球棍模型: |
C.OH-的电子式: |
| D.葡萄糖的结构简式:C6H12O6 |
最近我国科学家研究发现人体中微量的H2S能有效预防心脏病、老年性痴呆症。下列有关H2S的说法正确的是
| A.H2S属于非电解质 |
| B.人体内H2S可由含硫蛋白质降解产生 |
| C.大量吸入H2S对人体无害 |
| D.H2S只有还原性没有氧化性 |