某活动小组根据下图所示进行模拟炼铁的实验,并对产物的成分进行探究。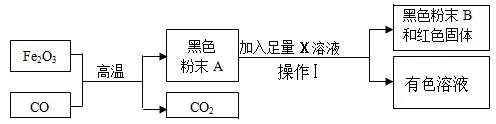
【提出问题】黑色粉末A可能是什么呢?
【查阅资料】小华查阅资料,得到关于铁的氧化物如下信息:
| 铁的氧化物 |
Fe2O3 |
Fe3O4 |
FeO |
| 颜色 |
红 |
黑 |
黑 |
| 物理性质 |
不能被磁铁吸引 |
能被磁铁吸引 |
不能被磁铁吸引 |
| 化学性质 |
可溶于酸 |
常温下不溶于稀酸 |
可溶于酸,但不生成气体 |
【提出猜想】(1)小明认为黑色粉末A全部是铁粉。为了证明自己的猜想小明设计了如上图的实验,该实验中,小明加入的X溶液是 ;实验过程中操作Ⅰ是 这个实验基本操作。
小华根据小明的实验认定小明的猜想是错误的,理由是 。
(2)小华根据资料提出了自己的两个猜想,请结合所学知识补充余下的一个猜想。
猜想①:黑色粉末A由铁粉和四氧化三铁(Fe3O4)组成
猜想②:黑色粉末A由铁粉和氧化亚铁(FeO)组成
猜想③:
【实验探究】
| 方案 |
实验操作 |
可能的现象 |
结论 |
| ① |
取适量黑色粉末A 用磁铁吸引 |
|
猜想①正确 |
| ② |
适量黑色粉末A 用磁铁吸引 |
黑色粉末部分被吸引 |
猜想②正确 |
| ③ |
|
|
猜想③正确 |
【反思评价】小娟认为方案②中得出的结论不正确,其理由是 。
【得出结论】黑色粉末A是铁和氧化亚铁的混合物。
小华想测定黑色粉末A中铁的质量分数,设计了如下实验:
取8g黑色粉末A加入50g足量的稀硫酸,充分反应后称量,剩余物质的质量为57.8g,则该黑色粉末A中铁的质量分数是多少?(写出计算过程)
(5分)某兴趣小组话动中,同学们按图1装置对“可燃物燃烧的条件”进行探究。探究过程中,发现白磷燃烧产生大量白烟,会刺激人体呼吸道,可能与空气中水蒸气反应,生成有毒的偏磷酸(HPO3)。已知白磷的着火点是40℃,红磷的着火点是240℃,请回答
(1)同学们对图1装置进行改进,按改进后的图2装置进行实验,改进后的装置优点是,不足是。
(2)请你帮助他们将下表补充完整。
| 现象 |
解释 |
| a试管中白磷燃烧,热水中白磷没有燃烧. b试管中红磷没有燃烧. |
b试管中红磷、热水中白磷都没有燃烧的原因是①; ②。 |
(3)能说明空气是混合物的实验现象为:实验结束后,图2装置保持原样。待a试管冷却后,如果将试管口紧贴水面(室温下)。热水中的白磷没有与氧气(或空气)接触。
小红同学想探究实验室中碳酸钙和盐酸制取二氧化碳后废液中溶质的成分,
请你一同参与探究并回答。
【提出问题】废液中的溶质是什么物质?
【作出猜想】小红认为废液中溶质只有CaCl2。
你认为废液中含有的溶质是(填化学式)。
【查阅资料】CaCl2溶液呈中性。
【实验与结论】
(1)请你写出碳酸钙和盐酸反应的化学方程式。
(2)分别取少量该废液和CaCl2溶液加入到两支试管中,并向其中分别滴入无色酚酞试液做对比试验,结果两支试管中溶液均无色,于是小红认为自己的猜想是正确的。
(3)你认为小红的实验(填“能”或“不能”)证明她的猜想。
(4)如果要证明你的猜想是正确的,你选择。(填字母:A、石蕊试液 B、氢氧化钠溶液 C、稀盐酸)来代替酚酞试液。现象是。
(5)为了防止这种废液造成环境污染,可以在废液中加入过量的充分反应后过滤,废液中就只剩一种溶质了。
实验室有几瓶未知浓度的氢氧化钠溶液,某兴趣小组同学欲用1%的稀盐酸来测定其溶质的质量分数。以下是几组同学的设想和做法:
(1)甲组同学的实验如下图所示:在烧杯中加入5g氢氧化钠溶液,滴入几滴酚酞溶液,用滴管慢慢滴入1%的稀盐酸,并不断搅拌,至溶液颜色恰好变为无色为止。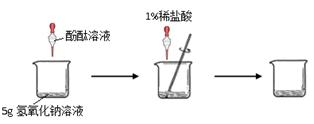
请回答:
①酚酞溶液的作用是;
②氢氧化钠与盐酸反应的化学方程式为;
③当溶液颜色恰好变为无色时,共用去了稀盐酸7.3g,试求甲组这瓶氢氧化钠溶液中溶质的质量分数和反应后所得溶液中溶质的质量分数(写出计算过程,结果用百分数表示)。
(2)乙组同学的设想是:在烧杯中加入一定量的氢氧化钠溶液,用滴管慢慢滴入1%的稀盐酸,并不断搅拌,通过用pH试纸多次测定溶液pH的办法,达到实验目的。
①下列使用pH试纸的方法正确的是(填字母)。
| A.将pH试纸剪成几段节约使用 |
| B.将pH试纸直接插入待测液中 |
| C.将pH试纸放在干净的白瓷板上,用玻璃棒蘸取待测液滴在pH试纸上 |
| D.将pH试纸用蒸馏水润湿后放在玻璃片上,用玻璃棒蘸取待测液滴在pH试纸上 |
②由于用pH试纸需多次测定,较繁琐,且所测数值不够精确。在老师指导下,乙组同学取了5g氢氧化钠溶液进行了数字化实验,由计算机描绘出了整个实验过程中溶液pH的变化图像(简单表示为下图)。
请回答:图中a点表示的含义是;b点溶液中的溶质有(填化学式);乙组同学要计算出本组这瓶氢氧化钠溶液中溶质的质量分数,除了要用到已有数据外,你认为还需要的数据是。
(3)丙组同学在滴加稀盐酸一段时间后,发现溶液中有少量气泡产生。这一“异常现象”激起了他们的探究欲望,通过实验证明:该组用的这瓶氢氧化钠溶液已经部分变质。请用化学方程式表示其变质的原因;
实验室有一瓶长期暴露在空气中的氢氧化钠固体,某兴趣小组的同学对该样品的成分及含量进行了探究。
【实验探究一】为得到纯净的氢氧化钠固体,并测定NaOH的纯度,设计的实验过程如下图。请回答下列问题: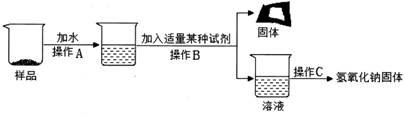
①长期暴露在空气中的氢氧化钠固体样品,所含杂质是(1),操作B中加入的试剂是(2);(以上填写化学式或物质名称均可)
②操作A、B 的名称分别为(3)、(4);
③若要测定该固体中NaOH的纯度,实验过程中一定还需用到的仪器是(5)。
【实验探究二】为了测定NaOH的纯度,小红同学设计如图装置(铁架台略去)。己知,碳酸氢钠溶液不吸收二氧化碳。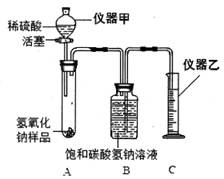
④写出指定仪器的名称:
甲(6)、乙(7);
⑤实验中取用样品质量要控制在一定范围内,如果样品用量过多,造成的后果是(8);
⑥取l0g样品进行实验,根据实验数据,通过计算可知产生了CO2 0.11g ,求原样品中NaOH的纯度,写出计算过程。
(9)【实验反思】
⑦利用该实验装置,若操作正确,装置气密性良好,测定的NaOH纯度也将(10)(填“偏大”或“偏小”),理由是(11)。
某化学兴趣小组在一次实验活动中发现钠能在二氧化碳中燃烧,他们对钠在二氧化碳气体中燃烧后生成的白色物质进行了如下探究:
实验:将燃烧的钠迅速伸入到盛满二氧化碳的集气瓶中,钠在其中继续燃烧至完全,反应后冷却,瓶底附着黑色颗粒,瓶壁上附着白色物质。
查资料:Na2O+H2O=2NaOH
提出假设:燃烧后瓶璧上附着的白色物质是什么?
假设1:白色物质是Na2O。
假设2:白色物质是Na2CO3
假设3:。
设计实验方案,验证假设
| 实验方案 |
实验操作 |
实验现象 |
结论 |
| 方案1 |
取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 |
溶液变成红色 |
白色物质是Na2O。 |
| 方案2 |
①取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入适量BaCL2 |
有白色沉淀生成 |
白色物质是Na2CO3 |
| ②静置片刻,取上层清液于试管中…… |
…… |
思考与交流:
(1)甲同学认为方案1得到的结论不正确,其理由是
(2)根据方案2的结论,补齐方案2中②的实验操作,并写出相应的实验现象。
实验操作:
实验现象:
(3)乙同学认为白色物质可能是NaOH,你填(同意或不同意)该同学的观点,
并简述理由:
(4)根据假设2,写出钠在二氧化碳中燃烧的化学方程式:。