阿伏加德罗常数的值约为6.02×1023,下列说法正确的是( )
A.l.8 g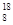 O2分子与1.8 g O2分子与1.8 g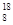 O3分子中含有的中子数不相同 O3分子中含有的中子数不相同 |
| B.标准状况下,22.4LCCl4中共价键数为4NA |
| C.80 mL 10 mol·L–1浓盐酸与足量MnO2反应,转移电子数为0.4×6.02×1023 |
| D.常温常压下,6.02×1023个SO3分子所占的质量约为80 g |
下列叙述中错误的是
| A.阿伏加德罗常数的数值与12g12C所含的碳原子数相等 |
| B.在0.5mol Na2SO4中,含有的Na+数约是6.02×1023 |
| C.等物质的量的O2与O3,所含氧原子数相等 |
| D.摩尔是物质的量的单位 |
下列关于金属性质的叙述中正确的是
| A.钠与氧气反应时,产物是由O2的用量决定的 |
| B.铝箔在空气中受热可以熔化且会发生剧燃烧 |
| C.金属与非金属单质发生反应时,被氧化的一定是金属 |
| D.铁丝不论在空气还是纯氧中都不会燃烧 |
下列事故或药品的处理正确的是
| A.一般用药匙取用粉末或块状药品 |
| B.当出现CO中毒时,应立即将中毒者抬到室外新鲜空气处 |
| C.制取并收集氧气结束后,应立即停止加热 |
| D.将含硫酸的废液倒入水槽,用水冲入下水道 |
下列图示与对应的叙述相符的是( )
| A.图1表示某放热反应在无催化剂(a)和有催化剂(b)时反应的能量变化,且加入催化剂改变反应的焓变 |
| B.图2表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20 mL Ba(OH)2溶液时铝离子恰好沉淀完全 |
| C.图3表示在CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b |
| D.图4表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应: |
2NO2(g) N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
海水中含有多种元素,开发利用这些资源是科学研究的重要课题。下图为海水利用的部分过程,下列有关说法正确的是( )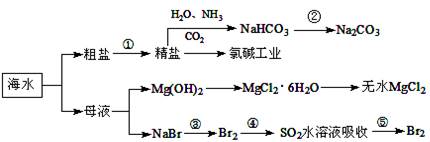
| A.要实现反应②可向NaHCO3溶液中加入过量石灰水 |
| B.氯碱工业中采用阴离子交换膜提高产品纯度 |
| C.MgCl2溶液加热蒸干可得无水MgCl2 |
| D.溴元素在反应③、⑤中均被氧化,在反应④中被还原 |