25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:
Sn(s)+Pb2+(aq) Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如下图所示。
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如下图所示。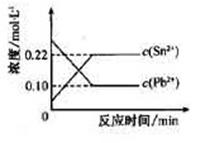
下列判断正确的是
| A.往平衡体系中加入金属铅后,c(Pb2+)增大 |
| B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小 |
| C.升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0 |
| D.25℃时,该反应的平衡常数K=2.2 |
不管化学反应过程是一步完成还是分为数步完成,这个过程的热效应是相同的。
已知:H2O(g)===H2O(l) ΔH1=-Q1 kJ/mol ①
C2H5OH(g)===C2H5OH(l) ΔH2=-Q2 kJ/mol ②
C2H5OH(g)+3O2(g)===2CO2(g)+3H2O(g) ΔH=-Q3 kJ/mol ③
若使23 g酒精液体完全燃烧,最后恢复到室温,则放出的热量为
| A.(Q1+Q2+Q3) kJ |
| B.[0.5(Q1+Q2+Q3)] kJ |
| C.(0.5Q1-1.5Q2+0.5Q3) kJ |
| D.(1.5Q1-0.5Q2+0.5Q3) kJ |
已知1 g氢气完全燃烧生成水蒸气时放出的热量121 kJ,且氧气中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中1 molH-O键形成时放出热量463 kJ,氢气中1 molH-H键断裂时吸收热量为
| A.920 kJ | B.557 kJ | C.436 kJ | D.188 kJ |
已知:
CH3CH2CH2CH3(g)+13/2O2(g) ===4CO2(g)+5H2O(l)ΔH=-2 878 kJ·mol-1
(CH3)2CHCH3(g)+13/2O2(g)===4CO2(g)+5H2O(l)ΔH=-2 869kJ·mol-1
下列说法正确的是
| A.正丁烷分子储存的能量大于异丁烷分子 |
| B.正丁烷的稳定性大于异丁烷 |
| C.异丁烷转化为正丁烷的过程是一个放热过程 |
| D.异丁烷分子中的碳氢键比正丁烷的多 |
已知下列两个热化学方程式
2H2(g) + O2(g) ===2H2O(l)△H = —571.6kJ·mol-1
C3H8(g) +5O2(g) === 3CO2(g) + 4H2O(l)△H = —2 220.0kJ·mol-1
实验测得氢气和丙烷的混和气体共5 mol完全燃烧时放热3847kJ,则混和气体中氢气与丙烷的体积比是
| A.1:3 | B.3:1 | C.1:4 | D.1:1 |
已知热化学方程式:
SO2(g)+1/2O2(g) 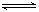 SO3(g) ΔH=-98.32 kJ/mol,在容器中充入2 mol SO2和1 mol O2充分反应,最终放出的热量为
SO3(g) ΔH=-98.32 kJ/mol,在容器中充入2 mol SO2和1 mol O2充分反应,最终放出的热量为
| A.196.64 kJ | B.196.64 kJ/mol | C.<196.64 kJ | D.>196.64 kJ |