人体正常血红蛋白中含有Fe2+,若误食亚硝酸盐,会导致Fe2+转化为Fe3+而中毒,服用维生素C可以解毒。对上述事实分析不正确的是
| A.亚硝酸盐是还原剂 | B.维生素C是氧化剂 |
| C.亚硝酸盐将Fe3+还原成Fe2+ | D.维生素C被Fe3+氧化 |
草酸(H2C2O4)是二元弱酸,草酸氢钠溶液显酸性。常温下向10mL 0.01mol/L NaHC2O4溶液中滴加0.01mol/L NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是
| A.V(NaOH) = 0时,c(H+)=1×10—2mol/L |
| B.V(NaOH) <10mL时,一定存在c(Na+)=c(C2O42-)+c(HC2O4--) |
| C.V(NaOH) =" 10" mL时,c(H+) = 1×10—7 mol/L |
| D.V(NaOH)>10 mL时,c(Na+)>c(C2O42-)>c(HC2O4-) |
在HNO3、Al(NO3)3和Mg(NO3)2的混合溶液中逐滴加入NaOH溶液,则消耗NaOH溶液的体积(x轴)与生成沉淀(y轴)之间的关系表示正确的是 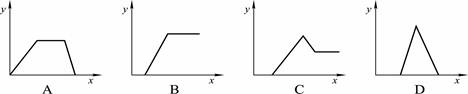
下列溶液中各微粒的浓度关系不正确的是
| A.0.1 mol/LCH3COOH溶液中:c(CH3COO-)+ c(CH3COOH)=0.1mol/L |
| B.CH3COONa溶液中:c(Na+)> c(CH3COO-)> c(OH-)> c(H+) |
| C.Na2S溶液中:2 c(Na+)= c(S2-) + c(HS-)+ c(H2S) |
| D.NaHCO3溶液中: c(OH-) = c(H+) + c(H2CO3)-c(CO32-) |
在t℃时,某NaOH稀溶液中,c(H+)=10-a mol/L,c(OH-)=10-b mol/L,已知a+b=13,则在该温度下,将100 mL 0.10 mol/L的稀硫酸与100 mL 0.40 mol/L的NaOH溶液混合后,溶液的pH为(已知:忽略混合时体积的变化;lg2=0.30;lg3=0.48)
| A.11.52 | B.11.70 |
| C.11.82 | D.12.00 |
下列各组离子能大量共存,且溶液为无色透明的是
| A.Al3+、AlO2-、NO3-、Cl- |
| B.CrO42-、H+、K+、NO3- |
| C.Ba2+、Na+、HCO3-、OH- |
| D.K+、SO42-、S2-、Na+ |