“套管实验”具有装置简洁便利等有优点,结合图示回答有关问题
(1)欲利用图1比较碳酸氢钠和碳酸钠的热稳定性,并检验分解产物。最好应在大试管底部加入 (填化学式),石灰水变浑浊的烧杯是 (填:甲、乙) 。
请写出试管中反应的化学反应方程式:
(2)使用图2中大小不一的试管,用铝粉和氢氧化钠溶液制取氢气,并收集一试管氢气,
将铝粉和氢氧化钠溶液放入 试管内(填:大、小)组成发生装置,请写出该反应的离子
方程式为: 为了使得所收集的氢气能较
纯净地充满所收集氢气的试管,应如何操作,写出大致的步骤:
。
 为了证明铜与稀硝酸反应产生的是NO,某校学生实验小组设计了一个实验,
为了证明铜与稀硝酸反应产生的是NO,某校学生实验小组设计了一个实验,
其装置如下图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,
内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的打气球。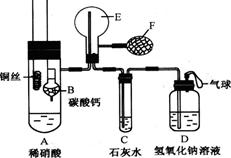
(1)实验时,为在E烧瓶中收集到NO,以便观察颜色,必须事先除去其中的空气。其中第一步实验操作为:。从装置的设计看,确定E中空气已被赶尽的实验现象是:______________。
(2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的离子方程式为。有人认为E中收集到的可能是H2而不是NO,如何证明?。
(3)实验过程中,发现在未鼓入空气的情况下,E中就产生红棕色。有人认为是由装置E部分设计不当造成的。你认为装置应改进的地方是。
(4)装置D的作用是。
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净,待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入20.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净,再用标准酸液润洗2-3次后,向其中注入0.1000 mol·L-1标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数。
③向锥形瓶中滴入酚酞作指示剂,进行滴定。滴定至指示剂刚好变色,且半分钟内颜色不再改变为止,测得所耗盐酸的体积为V1mL。
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2 mL。
试回答下列问题:
(1)终点时锥形瓶中的溶液从色变为 色。
(2)该小组在步骤①中的错误是,由此造成的测定
结果(偏高、偏低或无影响)。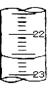
(3)上图,是某次滴定时的滴定管中的液面,其读数为mL。
(4)根据下列数据:
| 滴定次数 |
待测液体积(mL) |
标准盐酸体积(mL) |
|
| 滴定前读数(mL) |
滴定后读数(mL) |
||
| 第一次 |
20.00 |
0.50 |
25.40 |
| 第二次 |
20.00 |
4.00 |
29.10 |
请计算待测烧碱溶液的浓度为mol·L-1。
溴苯是一种用来合成医药、农药的重要原料,某化学课外活动小组用如图装置制取溴苯。先向分液漏斗中加入苯和液溴,在A下端活塞关闭的前提下,再将混合液慢慢滴入反应器A中。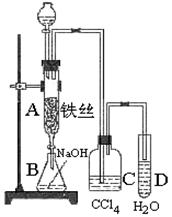
(1)写出A中反应的化学方程式
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是,C中盛放CCl4的作用是;
(3)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入溶液,现象是,则能证明;或者向试管D中加入溶液,现象是
已知非金 属单质硫(S)是淡黄色固体粉末,难溶于水。为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
属单质硫(S)是淡黄色固体粉末,难溶于水。为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
(1)装置A的分液漏斗中盛装的试剂是 ,烧瓶中加入的试剂是。
,烧瓶中加入的试剂是。
(2)画出虚线框内的实验装置图,并注明所加试剂,说明装置的作用。
(3)装置B中盛放的试剂是(选填下列所给试剂的代码),
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
化学反应方程式是。
(4)还有哪些事实能够说明氯元素的非金属性比硫元素的非金属性强(试举一例)。
(12分)某化学兴趣小组的同学用下图所示实验装置进行实验研究(图中a、b、c表示止水夹).请对其方案进行完善或评价;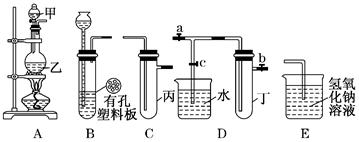
(1)实验室将B、C、E相连后,以、(填写名称)为原料可制取Cl2,为接下来研究氯气的化学性质做准备。
(2) 利用实验室常用方法制取氯气,将A、C、E相连,在丙中加入适量水,即可制得氯水.将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象、结论如下:
| 实验 序号 |
实验操作 |
现象 |
结论 |
| Ⅰ |
将氯水滴入品红溶液 |
品红溶液褪色 |
氯气与水反应的产物有漂白性 |
| Ⅱ |
氯水中加入碳酸氢钠粉末 |
有无色气 泡产生 |
氯气与水反应的产物具有酸性 |
请你评价:实验Ⅰ后,推出相应结论是否合理? ________________。若不合理,请说明理由(若合理,则无需填写下行):___________________________________________.
实验Ⅱ推出相应的结论是否合理? ________________若不合理,请说明理由(若合理,无需填写下行):____________________________________________________.
(3)A、C、E相连,可设计一个简单的实验,以验证Cl-和Br-的还原性强弱。有关反应的离子方程式为:____________________________________,
(4)B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),可制得并进行NO2有关实验.
①B中发生反应的化学方程式为___________________________
②欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹________,再打开止水夹________,使烧杯中的水进入试管丁的可能的操作是。