欲配制100 mL 1.0 mol/L Na2SO4溶液,正确的方法是:
① 将14.2 g Na2SO4 溶于100 mL水中
② 将32.2 g Na2SO4·10H2O溶于少量水中,再用水稀释至100 mL
③ 将20 mL 5.0 mol/L Na2SO4溶液用水稀释至100 mL
| A.①② | B.②③ | C.①③ | D.①②③ |
实验:①0.1 mol/L AgNO3溶液和0.1 mol/L NaCl溶液等体积混合得到浊液,过滤。
②分别取少量①的滤液,分别滴加等浓度等体积的饱和Na2S溶液、饱和Na2SO4溶液,前者出现浑浊,后者溶液仍澄清。
③取少量①的沉淀,滴加几滴氨水,沉淀逐渐溶解。
下列分析不正确的是
| A.实验②证明了①的滤液中含有Ag+,由此推断①的滤液中也含有Cl¯ |
| B.实验②证明了该温度下Ag2S比Ag2SO4更难溶解 |
| C.实验③的溶液中含有Ag(NH3)2+微粒 |
| D.由实验③推测:若在①的沉淀中滴加NaOH溶液,沉淀也能溶解 |
已知:某元素X的酸式盐(NaHX)溶液显碱性,下列说法正确的是
| A.NaHX的电离方程式为NaHX===Na+ + H+ + X2¯ |
| B.HX¯的电离程度小于HX¯的水解程度 |
| C.离子浓度关系:c(Na+) + c(H+) = c(OH¯) + c(HX¯) + c(X2¯) |
| D.加水稀释,促进HX¯水解,c(HX¯)增大 |
下列物质的制备线索中,不符合工业生产实际的是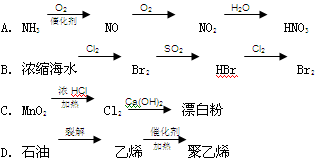
解释下列过程的方程式正确的是
A.氯化钠溶于水发生电离,电离方程式为:NaCl Na+ + Cl¯ Na+ + Cl¯ |
| B.用过量氨水吸收烟道气中的SO2:SO2+2NH3•H2O===SO32¯+2NH4++H2O |
C.工业冶炼金属铝:AlCl3(熔融) Al + Cl2↑ Al + Cl2↑ |
| D.向物质的量之比为1:1的NaOH和Na2CO3混合物中加入过量稀盐酸:OH¯+CO32¯+2H+===HCO3¯+H2O |
设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.1mol OH¯含有的电子数目为9NA |
| B.1mol Cl2和氢氧化钠完全反应,转移的电子数目为NA |
| C.室温下,1L pH=1的H2SO4溶液中,由水电离出的H+数目为0.1NA |
D.1mol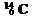 所含中子数目为6NA 所含中子数目为6NA |