(2分)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2F e(s)+3CO2(g) △H= ―24.8kJ/mol
e(s)+3CO2(g) △H= ―24.8kJ/mol
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H= ― 47.2kJ/mol
47.2kJ/mol
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:
_________________
下列说法中不正确的是()
| A.淀粉、纤维素、蛋白质都是天然高分子化合物 |
| B.开发核能、太阳能等新能源,推广乙醇汽油,使用无磷洗涤剂都可直接降低碳排放量 |
| C.花生油、豆油和牛油均属于高级脂肪酸甘油酯 |
| D.尼龙、棉花、天然橡胶、ABS树脂都是由高分子化合物组成的物质 |
某合金(仅含铜、铁)中铜和铁的物质的量之和为y mol,其中Cu的物质的量分数为a ,将其全部投入50 mL b mol·L-1的硝酸溶液中,加热使其充分反应(假设NO是唯一的还原产物)。下列说法正确的是
| A.若金属全部溶解,则溶液中一定含有Fe3+ |
| B.若金属有剩余,在溶液中再滴入硫酸后,金属又开始溶解 |
| C.若金属全部溶解,且产生336mL气体(标准状况),则b=0.3 |
| D.当溶液中金属离子只有Fe3+、Cu2+时,则a与b的关系为:b≥80y(1-a/3) |
用酸性氢氧燃料电池电解饱和食盐水的装置如图所示 (a、b为石墨电极)。下列说法中,正确的是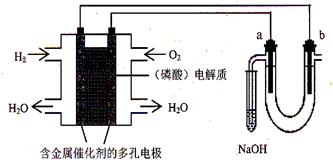
| A.电池工作时,正极反应式为:O2 +2 H2O + 4e-= 4OH- |
| B.电解时,a 电极周围首先放电的是Cl— |
| C.电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极 |
| D.忽略能量损耗,当电池中消耗0.2g H2 时,b极周围会产生2.24L H2 |
一定温度下, 将 2 mol SO2和 1 mol O2 充入一定容密闭容器中,在催化剂存在下进行下列反应: 2SO2(g)+ O2(g) 2SO3(g); △H= -197 kJ/ mol, 当达到平衡状态时, 下列说法中正确的是
2SO3(g); △H= -197 kJ/ mol, 当达到平衡状态时, 下列说法中正确的是
| A.生成 SO3为2 mol | B.反应放出 197 kJ 的热量 |
| C.SO2和 SO3 物质的量之和一定为 2mol | D.SO2的物质的量和SO3 物质的量一定相等 |
几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 |
X |
Y |
Z |
W |
| 原子半径/pm |
160 |
143 |
70 |
66 |
| 主要化合价 |
+2 |
+3 |
+5、+3、-3 |
-2 |
下列叙述正确的是()
A.X、Y元素的金属性 X > Y
B.Y单质与Z的最高价氧化物对应的水化物反应可制备氢气
C.Y的最高价氧化物对应的水化物能溶于氢氧化钠
D.一定条件下,Z单质与W的常见单质直接生成ZW2