“84”消毒液在日常生活中使用广泛,该消毒液无色,有漂白作用。它的有效成份是下列物质中的一种,这种物质是( )
| A.NaOH | B.KMnO4 | C.NaClO | D.Na2O2 |
能正确表示下列反应的离子方程式的是
A.以石墨为电极电解MgCl2溶液:2Cl-+2H2O H2↑+Cl2↑+2OH- H2↑+Cl2↑+2OH- |
B.NH4Cl水溶液显酸性:NH4++H2O=NH3 H2O+H+ H2O+H+ |
| C.AlCl3溶液中投入过量Na:Al3++4Na+2H2O=AlO2-+4Na++2 H2↑ |
| D.FeBr2溶液中通入少量Cl2:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
已知250C、101KPa下:①C(s)+ O2(g)="CO(g)" △H=
O2(g)="CO(g)" △H=  Q1kJ/mol②2 CO(g)+ O2(g)=2CO2(g)△H=
Q1kJ/mol②2 CO(g)+ O2(g)=2CO2(g)△H= Q2kJ/mol (Q1、Q2均为正数)据此推断,下列说法正确的是
Q2kJ/mol (Q1、Q2均为正数)据此推断,下列说法正确的是
A.碳的燃烧热为Q1kJ/mol
B.2molCO(g)所具有的能量一定高于2molCO2(g)所具有的能量
C.一定质量的碳燃烧,生成CO2(g)比生成 CO(g)时放出的热量多
D.碳燃烧生成CO2气体的热化学方程式为:C(s)+ O2(g)=CO2(g) △H=  (Q1+Q2)kJ/mol
(Q1+Q2)kJ/mol
用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.标准状况下,22.4LD2中含有2NA个中子 |
| B.常温常压下,3.36L氯气与2.7g铝充分反应,转移电子数为0.3NA |
| C.Cu-Zn-CuSO4原电池工作时,若析出0.1molCu时,转移电子数为0.2NA,正极溶解Zn6.5g |
| D.1mol异丁烷中,含共价键数目为10NA |
将Cu片放入0.1mol/LFeCl3溶液中,反应一定时间后取出Cu片,溶液中c(Fe3+):c(Fe2+)=2:3,则溶液中Cu2+与Fe3+的物质的量之比为
| A.3:2 | B.3:4 | C.3:5 | D.4:3 |
下列事实能说明甲酸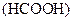 属于弱酸的是( )
属于弱酸的是( )
①1mol/LHCOOH的pH=2
②甲酸能与水以任意比互溶
③20mL 1mol/LHCOOH与20mL 1mol/LNaOH恰好中和
④HCOONa溶液的pH>7
| A.①② | B.②③ | C.③④ | D.①④ |