用食用白醋(醋酸浓度约1 mol/L)进行下列实验,能证明醋酸为弱电解质的是
| A.白醋中滴入石蕊试液呈红色 | B.实验测得该白醋的pH为2.3 |
| C.蛋壳浸泡在白醋中有气体放出 | D.白醋加入豆浆中有沉淀产生 |
由氧化铜、氧化铁组成的混合物ag,加入2 mol•L-1的硫酸50mL时固体恰好完全溶解,若取ag该混合物在足量的一氧化碳中加热充分,冷却后剩余固体质量为
| A.1.6g | B.(a-1.6)g | C.(a-3.2)g | D.无法计算 |
某同学用量筒液体时,将量筒平放,仰视液体凹液面最低处读数为16.0mL,倾倒出一部分溶液,又俯视液体凹液面最低处,读数为10.0mL,该同学取出液体的体积是
| A.大于6.0mL | B.等于6.0mL | C.小于6.0mL | D.无法判断 |
下列叙述不正确的是
A.溶质质量分数分别为a%和5a%的硫酸溶液按等体积混合,混合溶液中硫酸的质量分数大于3a%
B.将1体积cmol/L硫酸溶液用水稀释为5体积,得到0.2cmol/L硫酸溶液
C.10mL质量分数14%的氨水,用水稀释至100mL,氨水的质量分数小于1.4%
D将w g a% NaCl溶液蒸发掉w/2 g水,得到4a% NaCl溶液
a、b、c、d是HCl、BaCl2、AgNO3、Na2CO3四种溶液中的一种,现将它们两两混合,现象如下图所示
| 反应物 |
a+b |
c+d |
a+d |
a+c |
b+d |
| 现象 |
白色沉淀 |
白色沉淀 |
白色沉淀 |
白色沉淀 |
无色气体 |
由上述现象可推知a、b、c、d依次是
A.HCl、BaCl2、AgNO3、Na2CO3
B.AgNO3、HCl、Na2CO3、BaCl2
C.BaCl2、Na2CO3、AgNO3、HCl
D.AgNO3、HCl、BaCl2、Na2CO3
下列图示的四种实验操作对应描述正确的是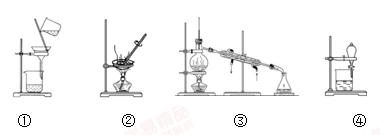
| A.除去KCl溶液中的K2CO3,加入适量Ca(NO3)2溶液,再用①装置分离 |
| B.用②装置除去自来水中的Cl-等杂质 |
| C.回收碘的CCl4溶液中的CCl4,可选用③装置 |
| D.分离水和植物油,选用④装置,下层的植物油可从分液漏斗的下层放出 |