下列各组中的离子,能在溶液中大量共存的是:
| A.K+、H+、SO42-、OH- | B.Na+、Ca2+、CO32-、NO3- |
| C.Na+、Cu2+、Cl-、SO42- | D.Na+、H+、Cl-、CO32- |
NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A.5.6 g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA |
| B.12.5mL 16mol·L-1浓硫酸与足量铜反应,转移电子数为0.2NA |
| C.7.8g Na2S和Na2O2的混合物中含有的阴离子数等于0.1NA |
| D.0.5mol雄黄(As4S4,结构如右图)含有NA个S—S键 |

分类是化学研究中常用的方法。下列分类方法中,不正确的是()
①根据元素原子最外层电子数的多少将元素分为金属和非金属
②根据电解质在水溶液中能否完全电离将电解质分为强电解质和弱电解质
③依据组成元素的种类,将纯净物分为单质和化合物
④根据酸分子中含有的氢原子个数,将酸分为一元酸、二元酸等
⑤根据氧化物中是否含有金属元素,将氧化物分为碱性氧化物、酸性氧化物
⑥根据分散系的稳定性大小,将分散系分为胶体、浊液和溶液
⑦依据有无电子转移,将化学反应分为氧化还原反应和非氧化还原反应
⑧根据化学反应的热效应,将化学反应分为放热反应、吸热反应
| A.①④⑤⑥ | B.③④⑤⑥ | C.只有①③ | D.全部正确 |
下列实验现象预测正确的是()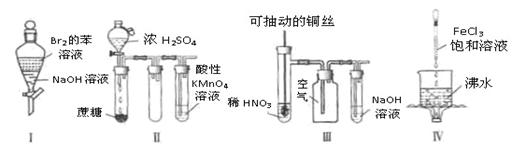
| A.实验I:振荡后静置,上层溶液颜色保持不变 |
| B.实验II:酸性KMnO4溶液中出现气泡,且颜色不变 |
| C.实验III:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 |
| D.实验IV:继续煮沸溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应 |
下列离子方程式书写正确的是()
| A.Na2S溶液水解:S2-+H2O=HS-+OH- |
| B.NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-=NH3↑+H2O |
| C.向酸性氯化亚铁溶液中加入过氧化氢溶液:2Fe2++H2O2+2H+=2Fe3++2H2O |
| D.铜与浓硝酸反应:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O |
下列各项操作中不发生先沉淀后沉淀溶解现象的是() ①向饱和Na2CO3溶液中通入过量CO2
①向饱和Na2CO3溶液中通入过量CO2 ②向Fe(OH)3胶体中逐滴滴入过量的H2SO4溶液
②向Fe(OH)3胶体中逐滴滴入过量的H2SO4溶液 ③向AgI胶体中逐滴加入过量稀盐酸
③向AgI胶体中逐滴加入过量稀盐酸 ④向石灰水中通入过量CO2
④向石灰水中通入过量CO2 ⑤向Na2SiO3溶液中滴入过量的盐酸
⑤向Na2SiO3溶液中滴入过量的盐酸
| A.①②③ | B.②③⑤ | C.①②③⑤ | D.①③⑤ |