下列说法或表示方法正确的是
| A.等物质的量的硫蒸气和固体硫分别完全燃烧,后者放出热量多 |
| B.由C(石墨)= C(金刚石);△H=+1.90 kJ/mol可知,金刚石比石墨稳定 |
| C.在101kPa时,2g氢气完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)= 2H2O(l) △H=-285.8kJ/mol |
D.在稀溶液中,H+(aq)+ OH-(aq) = H2O(l) △H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合, 放出的热大于57.3kJ 放出的热大于57.3kJ |
已知299 K时,合成氨反应 N2 (g ) + 3H2 ( g )  2NH3 ( g ) △H =" -92.0" kJ/mol,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应,达到平衡时,反应放出的热量为(忽略能量损失)
2NH3 ( g ) △H =" -92.0" kJ/mol,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应,达到平衡时,反应放出的热量为(忽略能量损失)
| A.一定小于92.0 kJ | B.一定等于92.0 kJ | C.不能确定 | D.一定大于92.0 kJ |
.金属镍有广泛的用途。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍(已知:氧化性Fe2+<Ni2+<Cu2+)。下列叙述正确的是
| A.阳极发生还原反应,其电极反应式:Ni2++2e-=Ni |
| B.电解过程中,阳极质量减少与阴极质量增加相等 |
| C.电解后,溶液中存在的金属阳离子只有Fe2+ 和 Zn2+ |
| D.电解后,电解槽底部的阳极泥中只有Cu和Pt |
CuCO3和Cu2(OH)2CO3的混合物34.6 g,可恰好完全溶解于300ml、2 mol.L-1的盐酸溶液中,加热分解等量的这种混合物可得CuO的质量()
| A.16.0 g | B.19.2 g | C.24.0 g | D.30.6 g |
下列溶液中能用来区别SO2和CO2气体的是
①澄清的石灰水 ②氢硫酸 ③氯水 ④酸性高锰酸钾溶液 ⑤氯化钡溶液 ⑥品红溶液
| A.①④⑤⑥ | B.②③④⑥ | C.①②③⑥ | D.②④⑤⑥ |
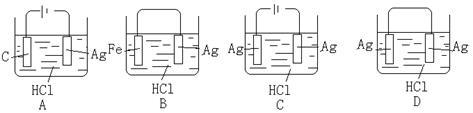
某学生欲完成2HCl+2Ag=2AgCl↓+H2↑反应,设计了下列四个实验,你认为可行的是