一定条件下,在体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应: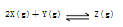 ,经60 s达到平衡生成0.3 mol Z,下列说法正确的是
,经60 s达到平衡生成0.3 mol Z,下列说法正确的是
| A.以X浓度变化表示的反应速率为0.001 mol/(L·s) |
| B.将容器体积变为20 L,Z的平衡浓度变为原来的1/2 |
| C.若增大压强,则物质Y的转化率减小 |
| D.若升高温度,X的体积分数增大,则该反应的DH>0 |
向盐酸中加入浓硫酸时产生白雾,下列叙述不属于产生该现象的原因是
| A.浓硫酸具有脱水性 | B.浓硫酸具有吸水性 |
| C.盐酸具有挥发性 | D.气体的溶解度随温度升高而降低 |
欲迅速除去水壶底的水垢,又不损坏铝壶,最好选用
| A.浓盐酸 | B.稀硝酸 | C.冷的浓硫酸 | D.冷的浓硝酸 |
只用一种试剂就能把Na2SO4、NaCl、(NH4)2SO4、NH4Cl四种溶液区分开来,这种试剂是
| A.AgNO3 | B.NaOH | C.BaCl2 | D.Ba(OH)2 |
用一种试剂证明生石灰中含有石灰石和石英,下列试剂适宜的是
| A.盐酸 | B.硫酸 | C.NaOH溶液 | D.氯化钠溶液 |
下列试剂能贮存在磨口玻璃塞的试剂瓶里的是
| A.HF溶液 | B.KOH溶液 | C.盐酸 | D.水玻璃 |