在一定温度下,向足量的饱和硫酸铜溶液中加入1.60g无水硫酸铜粉未,搅拌后静置,最终所得的晶体(CuSO4·5H2O)的质量是()
| A.等于1.60g | B.大于1.60g,小于2.50g |
| C.等于2.50g | D.大于2.50g |
下列说法错误的是()
| A.作半导体材料的元素大多数位于周期表中金属和非金属的交界处 |
| B.农药中常含有的元素通常在元素周期表的右上方区域内 |
| C.作催化剂材料的元素通常在元素周期表的左下方区域内 |
| D.在周期表过渡元素第ⅢB族到ⅥB族中,可寻找到耐高温和耐腐蚀的合金材料 |
下列化学用语表述正确的是()
A.Cl-的结构示意图 |
B.MgCl2的电子式 |
C.CCl4的结构式 |
D.高碘酸的分子式 H4IO5 |
X、Y、Z三种元素的电子层数相同,它们的最高价氧化物分别为酸性氧化物、碱性氧化物、两性氧化物,则三种元素原子序数的大小顺序为()
| A.X>Y>Z | B.Y>X>Z | C.X>Z>Y | D.Z>X>Y |
下列各分子中所有原子都满足最外层为8电子结构的是( )
| A.BeCl2 | B.PCl3 | C.PCl5 | D.N2 |
在强酸性溶液中,下列各组离子能大量共存的是()
A.Na 、Ba 、Ba 、NO 、NO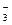 、Cl 、Cl |
B.Na 、Cl-、NO 、Cl-、NO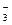 、Ag 、Ag |
C.NH 、Na 、Na 、SO 、SO 、CO 、CO |
D.Na 、MnO 、MnO 、Cl 、Cl 、K 、K |