设NA为阿伏加德罗常数,则下列说法不正确的是
| A.在标准状态下,2.24L己烷含有的氢原子数目为1.4NA |
| B.1.6g甲烷完全燃烧生成二氧化碳和水,转移的电子数为0.8NA |
| C.14g乙烯和环丙烷混合物中含有的碳原子数目为NA |
| D.0.1mol乙炔分子中含有的共用电子对数目为0.5NA |
有三种不同取代基 ,
,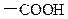 ,
,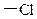 ,当它们同时取代苯分子中的3个氢原子,且每种取代产物中,只有两个取代基相邻时,取代产物有()
,当它们同时取代苯分子中的3个氢原子,且每种取代产物中,只有两个取代基相邻时,取代产物有()
| A.2种 | B.4种 | C.6种 | D.8种 |
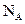 表示阿伏加德罗常数,下列说法中正确的是()
表示阿伏加德罗常数,下列说法中正确的是()
A. 铁粉与一定量的稀硝酸充分反应,转移电子数一定是 铁粉与一定量的稀硝酸充分反应,转移电子数一定是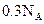 |
B.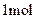 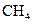 和 和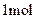 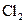 在光照的情况下充分反应,生成 在光照的情况下充分反应,生成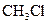 分子数为 分子数为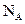 |
C.常温下,某酸溶液中酸根离子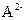 数为 数为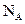 ,则 ,则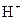 离子数一定是 离子数一定是 |
D.常温常压下,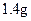 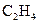 和 和 的混合气体中含有原子总数为 的混合气体中含有原子总数为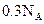 |
关于下列四个图象的说法中正确的是()
A.图①表示可逆反应“  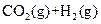 ”中的 ”中的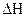 小于0 小于0 |
| B.图②是在电解氯化钠稀溶液的电解池中,阴、阳极能收集到的气体体积之比一定为1:1 |
C.图③表示可逆反应  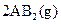 的 的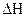 大于0 大于0 |
D.图④表示压强对可逆反应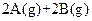  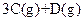 的影响,乙的压强大 的影响,乙的压强大 |
化学与生活、社会密切相关。下列说法不正确的是()
| A.低碳生活要求节能减排,尽量使用太阳能等代替化石燃料,减少温室气体的排放 |
| B.聚氯乙烯不能使溴的四氯化碳溶液褪色 |
| C.为了减少“白色污染”,我国规定商家不得无偿提供塑料袋 |
D.三聚氰胺(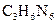 )含氮量很高,可作为牛奶添加剂 )含氮量很高,可作为牛奶添加剂 |
铅蓄电池的两极分别为Pb、PbO2,电解质溶液为H2SO4,工作时的反应为
Pb+PbO2+2H2SO4=2PbSO4+2H2O,下列结论不正确的是
| A.Pb为负极被氧化 | B.外电路有2 mol电子转移时,负极消耗 SO42-为2 mol |
| C.溶液的pH不断减小 | D.电解质溶液pH不断增大 |