某溶液中含有两种溶质NaCl和H2SO4,它们的物质的量之比为1︰1。用石墨做电极电解该溶液时,下列叙述不正确的是
| A.阴极只析出H2 | B.阳极先析出Cl2,后析出O2 |
| C.电解最后阶段为电解水 | D.溶液pH不断增大,最后为7 |
用NA表示阿伏加德罗常数。下列叙述正确的是
| A.100mL3mol/L盐酸与5.6gFe充分反应转移0.3NA个电子 |
| B.6g尿素与葡萄糖的混合物在足量氧气中完全燃烧生成0.2NA个水分子 |
C.12gC60( )中含有NA个共价键 )中含有NA个共价键 |
| D.10mL5mol/L(NH4)2SO4溶液中含有NH4+数目为0.1NA个 |
下列离子方程式书写正确的是
A.用惰性电极电解硫酸铜溶液: Cu2+ +2OH- Cu↓ + H2↑+O2↑ Cu↓ + H2↑+O2↑ |
| B.氨气通入饱和碳酸氢钠溶液中:H+ + NH3 = NH4+ |
| C.铝溶于氢氧化钠溶液中,2Al +2OH-+2H2O=2AlO2-+3H2↑ |
D.溴乙烷与6mol/L氢氧化钠水溶液共热:C2H5Br +OH-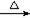 CH2=CH2↑+Br-+H2O CH2=CH2↑+Br-+H2O |
海底黑烟囱可在海底堆积硫化物的颗粒,形成多种金属矿产。若从海底黑烟囱附近的矿产物中分离出富铜矿CuFeS2,可用于冶炼铜,熔炼过程主要反应为:
2CuFeS2─→Cu2S+2FeS+S……………………………①
2Cu2S+3O2=2Cu2O+2SO2………………………………… ②
Cu2O+FeS─→Cu2S+FeO……………………………… ③
2FeS+3O2+SiO2─→2FeO·SiO2+2SO2………………… ④
2FeO+SiO2─→2FeO·SiO2……………………………… ⑤
Cu2S+2Cu2O─→6Cu +SO2 ……………………………… ⑥
下列有关说法不正确的是
| A.上述反应均属于氧化还原反应 | B.该厂可同时建硫酸厂和炼铁厂 |
| C.该厂的原料除富铜矿外,还需空气和硅石 | D.反应④转移12e- |
反应A+3B=2C,若7gA与一定量的B完全反应生成8.5gC,则A、B、C的相对分子质量之比( )
A.14:3:17 B. 28:2:17
C.1:3:2 D. 无法确定
V mL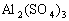 溶液中含
溶液中含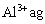 ,取
,取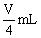 溶液稀释到4VmL,则稀释后溶液中
溶液稀释到4VmL,则稀释后溶液中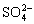 的物质的量浓度是()
的物质的量浓度是()
A. |
B.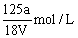 |
C.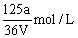 |
D.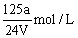 |