电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
(1)若X、Y都是惰性电极,a是AgNO3溶液,实验开始时,同时在两边各滴入几滴
石蕊试液,则
①电解池中X极上的电极反应式为 ,
②Y电极上的电极反应式为 ,在Y极附近观察到的现象是 。
③电解总反应方程式为 。
(2)如X是金属铁,要在铁件的表面镀铜防止铁被腐蚀,则
①Y电极的材料是 ,电极反应式是 。电解液a选用  溶液。电解过程中其浓度 (增大、减小或不变)
溶液。电解过程中其浓度 (增大、减小或不变)
②若电镀前X、Y两电极的质量相同,电 镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12 g,则电镀时电路中通过的电子为_______mol。
镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12 g,则电镀时电路中通过的电子为_______mol。
③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因
。
下列所含分子数由多到少的排列顺序是 。
| A.标准状况下33.6 L H2 |
| B.所含电子的物质的量为4 mol的H2 |
| C.20 ℃时45 g H2O |
| D.常温下,16 g O2与14 g N2的混合气体 |
E.含原子总数约为1.204×1024的NH3
现有m g某气体,它由双原子分子构成,它的摩尔质量为M g/mol。若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为________mol。(2)该气体所含原子总数为__________个。
(3)该气体在标准状况下的体积为____________L。
(4)该气体溶于1 L水中(不考虑反应),其溶液中溶质的质量分数为__ ___。
(5)该气体溶于水后形成V L溶液,其溶液的物质的量浓度为___ __mol/L。
化学试剂应根据其性质和形态进行有效妥善保存:固体试剂应保存在 ,液体试剂保存在 ,见光易分解的试剂(如:浓HNO3、AgNO3等)应用 色试剂瓶保存。氢氟酸(HF)因和玻璃中的SiO2强烈反应而腐蚀玻璃,应用 存放;金属钠、钾应保存在 中;少量白磷应该保存在 中。
(12 分)现向含6 mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图所示。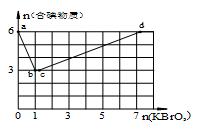
已知①BrO3-+6I一+6H+=3I2+Br-+3H2O;
②2BrO3- +I2 = 2IO3-+ Br2;
请回答下列问题:
(1)由反应②有同学由此得出氧化性:I2>Br2的结论,你认为是否正确 (填是或否),并说明理由 。
(2)b点时,KI反应完全,则消耗的氧化剂与还原剂物质的量之比为 ,还原产物是 。
(3)b→c过程中只有一种元素的化合价发生变化,写出该过程的离子反应方程式 。
(4)含6 mol KI的硫酸溶液所能消耗n(KBrO3)的最大值为 mol。
(5)n(KBrO3)=4时,对应含碘物质的化学式为 。
(11 分)无水AlCl3易升华,可用作有机合成的催化剂等,工业上由铝土矿(主要成分是Al2O3和Fe2O3,还含有少量的SiO2 )和石油焦(主要成分是C)为原料制备无水AlCl3:2Al2O3+6Cl2===4AlCl3+3O2
回答以下问题:
(1)加入焦炭后的化学反应可表示为Al2O3+C+Cl2 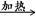 AlCl3+X↑,设计实验确定气体X的成分:__________。
AlCl3+X↑,设计实验确定气体X的成分:__________。
(2)在提纯AlCl3粗产品时,需加入少量铝粉,可使熔点较低的FeCl3转化为熔点较高的FeCl2,从而避免在AlCl3中混入铁的氯化物。该反应的化学方程式为____________________。
(3)为测定制得的无水AlCl3产品(含FeCl3杂质)的纯度,称取16.25 g无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,残留固体质量为0.32 g。
①过程涉及的离子方程式___________________、_______________。
②AlCl3产品的纯度为__________________________________。