下列各组离子,在溶液中能大量共存,加入NaOH溶液后加热既有气体放出又有沉淀生成的一组是( )
| A.Ba2+、NO3-、NH4+、Cl- | B.Ca2+、HCO3-、NH4+、AlO2- |
| C.K+、Ba2+、Cl-、HS O3- | D.Mg2+、NH4+、SO42-、K+ |
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=" +" 49.0 kJ·mol-1
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g);△H=-192.9 kJ·mol-1
下列说法正确的是()
| A.CH3OH的燃烧热为192.9 kJ·mol-1 |
B.反应①中的能量变化如图所示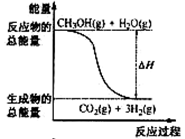 |
| C.CH3OH转变成H2的过程一定要吸收能量 |
| D.根据②推知反应:CH3OH(l)+1/2O2(g)=CO2(g)+ 2H2(g)的△H>-192.9kJ·mol-1 |
在一密闭容器中进行下列反应:2SO2(g) + O2(g)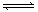 2SO3(g),已知反应过程中某一段时刻SO2,O2,SO3的浓度分别为0.2mol/L,0.1mol/L,0.2mol/L,当反应达到平衡时,可能存在的数据是()
2SO3(g),已知反应过程中某一段时刻SO2,O2,SO3的浓度分别为0.2mol/L,0.1mol/L,0.2mol/L,当反应达到平衡时,可能存在的数据是()
| A.SO2为0.4mol/L,O2为0.2mol/L | B.SO2为0.25mol/L |
| C.SO2,SO3均为0.15mol/L | D.SO3为0.4mol/L |
可以证明可逆反应N2(g) + 3H2(g) 2NH3(g)已达到平衡状态的是:()
2NH3(g)已达到平衡状态的是:()
①一个N≡N断裂的同时,有3个H-H键断裂②一个N≡N键断裂的同时,有6个N-H键断裂③其它条件不变时,混合气体平均式量不再改变④保持其它条件不变时,体系压强不再改变⑤NH3%、N2%、H2%都不再改变⑥恒温恒容时,密度保持不变⑦正反应速率v(H2)=0.6mol/L·min,逆反应速率v(NH3)=0.4mol/L·min
| A.全部 | B.只有①③④⑤ | C.②③④⑤⑦ | D.只有①③⑤⑥⑦ |
在一密闭烧瓶中充满NO2,在25℃时NO2与N2O4达到平衡: 2NO2(g) N2O4(g)ΔH﹤0把烧瓶置于100℃沸水中,又建立新的平衡状态,前后两平衡比较,不变的是()
N2O4(g)ΔH﹤0把烧瓶置于100℃沸水中,又建立新的平衡状态,前后两平衡比较,不变的是()
| A.颜色 | B.平均分子量 | C.物质的量 | D.密度 |
一定量的锌粉和6 mol/L的过量盐酸反应,当向其中加入少量的下列物质时,能够加快反应速率,又不影响产生H2的总量的是 ( )
①石墨粉 ②CuO ③铜粉 ④铁粉 ⑤浓盐酸
| A.①②⑤ | B.①③⑤ | C.③④⑤ | D.①③④ |