向某盐溶液中通入过量Cl2,滴加Ba(NO3)2溶液和稀硝酸,有白色沉淀生成,则原溶液可能是( )
| A.AlCl3溶液 | B.CaCl2溶液 | C.Na2SO3溶液 | D.Na2CO3溶液 |
下表各组物质中,物质之间不可能实现如图所示转化的是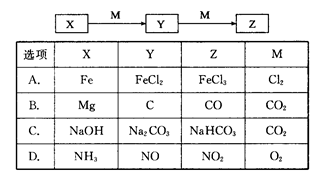
下列离子方程式的书写正确的是
| A.水玻璃中通入过量二氧化碳:Na2SiO3+CO2+H2O=2Na++CO32-+H2SiO3 |
| B.澄清石灰水中通入过量二氧化碳:Ca(OH)2+2CO2=Ca2++2HCO3- |
| C.硅与氢氟酸的反应:Si+4H++4F-=SiF4↑+2H2↑ |
| D.二氧化硅溶于烧碱溶液中:SiO2+2OH-=SiO32-+H2O |
某同学用以下装置制备并检验Cl2的性质。下列说法正确的是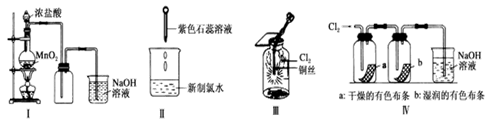
| A.Ⅰ图:若浓盐酸过量,则理论上MnO2可全部消耗完 |
| B.Ⅱ图:证明新制氯水只具有酸性 |
| C.Ⅲ图:产生了棕黄色的雾 |
| D.Ⅳ图:湿润的有色布条褪色,说明氯气具有漂白性 |
室温下,下列各组离子能大量共存的是
| A.稀硫酸中:K+、Mg2+、AlO2-、S2O32- |
| B.Na2S溶液中:SO42-、K+、Cl-、Cu2+ |
| C.Kw/c(H+)=10-13溶液中:Fe3+、NH4+ 、Mg2+、SO42- |
| D.通人大量CO2的溶液中:Na+、ClO-、CH3COO-、HCO3- |
对下列事实的解释正确的是
| A.浓硝酸通常保存在棕色的试剂瓶中,说明浓硝酸不稳定 |
| B.浓硫酸具有吸水性,说明可用浓硫酸干燥氨气 |
| C.足量铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化Fe2+ |
| D.常温下,可用铝制容器盛装浓硫酸,说明浓硫酸与铝不反应 |