下列说法正确的是
| A.酸雨样品露天放置一段时间,酸性增强,是由于雨水所含成分被氧化的原因 |
| B.N、P、As的非金属性逐渐增强 |
| C.因为氧化性HClO>稀H2SO4,所以非金属性Cl>S |
| D.钠原子在反应中失去的电子比铝原子少,故钠的金属性应弱于铝 |
室温下10mL0.1mol/L的醋酸溶液加水稀释后,下列说法正确的是()
| A.溶液中导电粒子的数目减少 |
B.溶液中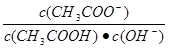 不变 不变 |
| C.醋酸的电离程度增大,c(H+)也增大 |
| D.再加入10mL0.1mol/L的NaOH溶液,混合液的pH=7 |
下列说法或表示方法正确的是()
| A.等质量的硫蒸气和硫磺分别完全燃烧,二者放出的热量一样多 |
| B.氢气的燃烧热为285.8kJ/mol,则氢气燃烧的热化学方程式为 2H2(g)+O2(g)=2H2O(l) ∆H="-285.8" kJ/mol |
| C.2H2(g)+O2(g)=2H2O(l) ∆H=-Q1 kJ/mol 2H2(g)+O2(g)=2H2O(g) ∆H=-Q2 kJ/mol,则Q1>Q2 |
| D.已知中和热为57.3 kJ/mol,若将含0.5molH2SO4的浓溶液与含1molNaOH的溶液混合,放出的热量等于57.3kJ |
下列说法不正确的是()
| A.用10mL量筒量取6.8mL稀H2SO4 |
| B.用碱式滴定管量取15.80mLKMnO4溶液 |
| C.酸碱中和滴定时,滴定管需用标准液或待测液润洗 |
| D.中和热测定时,氢氧化钠溶液稍过量的目的是为了保证盐酸完全被中和 |
已知4NH3(g)+5O2(g)=4NO(g)+6H2O(g),若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则下列关系正确的是()
| A.4 v(NH3)="5" v(O2) | B.5v(O2)="6" v(H2O) |
| C.2 v(NH3)="3" v(H2O) | D.4v(O2)=" 5" v(NO) |
下列物质在水溶液中的电离方程式正确的是()
| A.H2SO4=2H++SO42- | B.NaHCO3 Na++HCO3- Na++HCO3- |
C.Na2CO3 2Na++CO32- 2Na++CO32- |
D.CH3COOH=H++CH3COO- |