下列反应中属于氧化还原反应的是( )
| A.CO2+H2O==H2CO3 | B.H2CO3==CO2↑+H2O |
| C.CaCO3+2HCl==CaCl2+H2O+CO2↑ | D.CO2+C高温2CO |
有关能量的判断或表示方法正确的是()
| A.由:H++OH—→H2O+57.3KJ,可知:含0.5mol H2SO4的浓溶液与含1molNaOH的溶液混合,放热量大于57.5KJ |
| B.从C(石墨)→C(金刚石)-119KJ,可知:金刚石比石墨更稳定 |
| C.等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量更多 |
| D.2gH2完全燃烧生成液态水放出285.8KJ热量,则氢气燃烧的热化学方程式为: |
2H2(g)+O2(g)→2H2O(1)+285.8KJ
下列实验能达到预期目的的是( )
| 编号 |
实验内容 |
实验目的 |
||
|
由部分短周期元素形成的单质或氧化物之间有以下关系
单质X + 氧化物M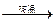 氧化物N
氧化物N
单质Y + 氧化物M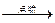 单质X + 氧化物R
单质X + 氧化物R
单质X + 氧化物Z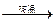 单质D + 氧化物N
单质D + 氧化物N
若X为非金属单质,则组成Y单质的元素在周期表的位置是
| A.第二周期ⅣA族 | B.第二周期ⅥA族 |
| C.第三周期ⅡA族 | D.第三周期ⅣA族 |
常温时,有浓度均为0.1 mol/L的四种溶液:①Na2CO3溶液②NaHCO3溶液③盐酸④氨水,下列有关说法不正确的是()
| A.上述溶液中,既能与NaOH反应,又能与H2SO4反应的溶液中离子浓度由大到小的顺序为:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+) |
| B.向④中加入少量的NH4Cl固体,此时溶液中c(NH4+)/c(OH-)的值增大 |
| C.若将③和④的溶液混合后,溶液恰好呈中性,则混合前溶液的体积为③<④ |
| D.取10 mL溶液③,加水稀释到100 mL,此时溶液中由水电离的c(H+) = 1×10-12mol/L |
有下列六种转化途径,某些反应条件和产物已省略,下列有关说法正确的是()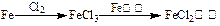
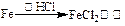 途径①
途径①
途径②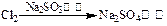 途径③
途径③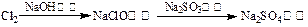 途径④
途径④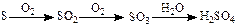
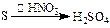 途径⑤
途径⑤
途径⑥
| A.由途径①和②分别制取1 mol FeCl2,理论上各消耗1 mol Fe,各转移2 mol e- |
| B.由途径③和④分别制取1 mol Na2SO4,理论上各消耗1 mol Cl2,各转移2 mol e- |
| C.由途径⑤和⑥分别制取1 mol H2SO4,理论上各消耗1 mol S,各转移6 mol e- |
| D.以上说法都不正确 |