下列说法中错误的是( )
| A.置换反应一定是氧化还原反应 |
| B.化合反应不可能是氧化还原反应 |
| C.分解反应可能是氧化还原反应 |
| D.凡是氧化还原反应,都不可能是复分解反应 |
以下进行性质比较的实验,不合理的是
| A.比较Cu、Fe2+的还原性:铁加入硫酸铜溶液中 |
| B.比较氯、溴单质的氧化性:溴化钠溶液中通入氯气 |
| C.比较镁、铝金属性:氯化镁、氯化铝溶液中分别加入过量的NaOH溶液 |
| D.比较碳、硫非金属性:测定同条件同物质的量浓度的Na2CO3、Na2SO4溶液的pH |
海水中主要含有Na+、K+、Mg2+、Ca2+、Cl-、Br-、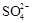 、
、 、
、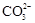 等离子,火力发电时排放的烟气可用海水脱硫,其工艺流程如下图所示:
等离子,火力发电时排放的烟气可用海水脱硫,其工艺流程如下图所示: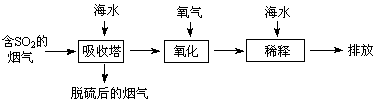
下列说法错误的是
A.海水pH约为8的原因主要是天然海水含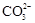 、 、 |
B.吸收塔中发生的反应有SO2+H2O H2SO3 H2SO3 |
C.氧化主要是氧气将 、 、 、H2SO3氧化为 、H2SO3氧化为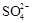 |
D.经稀释“排放”出的废水中,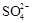 浓度与海水相同 浓度与海水相同 |
“酸化”是实验中经常采用的方法,下列酸化过程正确的是
| A.抑制Fe2+的水解,用稀硝酸酸化 |
| B.提高高锰酸钾的氧化能力,用盐酸酸化 |
C.确认溶液中含有 时,先用盐酸酸化,再检验 时,先用盐酸酸化,再检验 |
| D.检验氯乙烷中的氯元素,加碱溶液加热后,用稀硫酸酸化后,再检验 |
从海带中提取碘的实验过程中,涉及到下列操作,其中正确的是
| A.放出碘的苯溶液 | B.氧化I- | C.将海带灼烧 | D.过滤含I-溶液 |
下列说法不正确的是
| A.分子式为C5H10O2的羧酸共有3种 |
| B.分子式为C3H9N的异构体共有4个 |
| C.某烷烃CnH2n+2的一个分子中,含有共价键的数目是3n+1 |
| D.某烷烃CnH2n+2的一个分子中,含有非极性键的数目是n-1 |