(共14分)右图中,A为空气中常见的气体单质、B、C、E是金属单质,D为非金属单质。已知:①I是一种常见的温室气体,E原子核内有12个质子②反应 能放出大量的热,该反应曾应用于铁轨的焊接;回答下列问题:
能放出大量的热,该反应曾应用于铁轨的焊接;回答下列问题: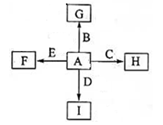
(1)分别写出F、G、H、I的化学式
F G H I
(2)书写下列化学方程式 ;
;
(3)C与NaOH溶液反应的化学方程式为 ,
反应后溶液与过量化合物I反应的化学方程式为 ;
⑷1.6gG溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需的铜粉的质量为:
(提示 :2FeCl3 + Cu ==2FeCl2+ CuCl2);
如何鉴别一种白色固体粉末是碳酸氢钠还是碳酸钠?(步骤、现象、结论)
_______________________________________________________________。
(本题6分)
⑴电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
①检验溶液中Fe3+存在的试剂是 __,证明Fe3+存在的现象是 __。[来]②写出FeCl3溶液与金属铜发生反应的化学方程式:。
⑵ 3Cl2+ 6NaOH ="=" 5NaCl + NaClO3+ 3H2O
氧化剂与还原剂的物质的量之比为,氧化产物是 ________。
室温下,A是常见的金属单质、单质B是黄绿色气体、单质C是无色气体。在合适反应条件下,它们可以按下面框图进行反应;E是无色溶液,F是淡绿色溶液。B和C反应发出苍白色火焰。请回答:(本题9分)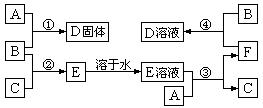
(1)A是__________,B是__________,C是__________(请填写化学式);
(2)反应①的化学方程式______________________________;
(3)反应③的离子方程式______________________________;
(4)反应④的离子方程式______________________________。
写出下列反应的化学方程式或离子方程式:(本题8分)
⑴氯化铁溶液中加入铁粉
化学方程式:____________________________________
⑵碳酸氢钠溶液滴入盐酸中
离子方程式:________________________________________
⑶碳酸氢钠溶液和氢氧化钠溶液反应
化学方程式:________________________________________
⑷将二氧化碳通入炽热的炭层
化学方程式:________________________________________
填写下列空格(本题3分)
| 化学反应方程式 |
氧化剂 |
还原剂 |
| Zn + 2HCl = ZnCl2 + H2↑ |
||
| 3NO2 + H2O= 2HNO3+ NO |
||
C+H2O(气)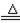 CO+H2 CO+H2 |