一定条件下,体积为2L的密闭容器中,1mol A和1mo1 B进行反应:
A(g)+3B(g)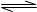 2C(g) 经2分钟反应达到平衡,此时生成0.2mol C。
2C(g) 经2分钟反应达到平衡,此时生成0.2mol C。
下列说法正确的是 ( )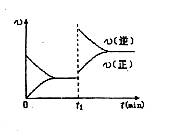
A.反应开始至2分钟时,以B浓度变化表示的反应速率为0.05mol/(L.min)
B.反应开始至2分钟时,A的转化率为5%
C.若其他条件不变,升高温度,A的体积分数增大,则该反应的△H<0
D.若其他条件不变,增大压强,化学反应速率的变化符合右侧示意图
常温下,下列对有关溶液的判断不正确的是()
| A.Na2CO3溶液中,c(OH-) = c(H+)+c(HCO3–)+c(H2CO3) |
B.温度相同、浓度相同的①(NH4)2SO4、②NaNO3、③NH4HSO4、④NH4NO3、⑤ 、⑥CH3COONa溶液,它们的pH值由小到大的排列顺序是:③①④②⑥⑤ 、⑥CH3COONa溶液,它们的pH值由小到大的排列顺序是:③①④②⑥⑤ |
| C.NaA溶液的pH=8,c(Na+)-c(A-) = 0.99×10-6 mol/L |
| D.10 mL pH = 12的氢氧化钠溶液中加入pH = 2的HA至pH刚好等于7,所得溶液体积V(总)≤20mL |
T °C时,在2 L密闭容器中,X、Y、Z三种气体的物质的量随时间变化如下图I所示。若起始时加入一定量的Y,在不同温度下改变X的量时Z的体积分数变化情况如图II所示。则下列结论正确的是
A.该反应的化学方程式为: 2X(g) + Y(g)  2Z(g) 2Z(g) |
| B.反应进行的前3min内,用X表示的平均反应速率v(x)=0.067mol/(L·min) |
| C.由图II可知,其他条件不变,增大X的量时Y的转化率先增大后减小 |
| D.其他条件不变,升髙温度,平衡逆向移动 |
强电解质甲、乙、丙、丁分别溶于水,电离出NH4+、Ba2+、Mg2+、H+、OH-、Cl-、
HCO3-、SO42-(每种溶液中溶质电离出的离子各不相同)。已知:①甲溶液分别与其它三种溶液混合,均产生白色沉淀;② 0.1 mol·L-1乙溶液中c(H+)>0.1 mol·L-1;③向丙溶液中滴入AgNO3溶液,产生不溶于稀HNO3的白色沉淀。下列结论不正确的是
| A.四种物质中一定有共价化合物 | B.四种物质中一定有Ba(OH)2 |
| C.丙溶液中含有NH4+ | D.丁溶液中含有HCO3- |
某种激光染料,应用于可调谐染料激光器,它由C、H、O三种元素组成,分子球棍型如右图所示,下列有关叙述正确的是
① 能与溴水发生取代反应②能使酸性KMn04溶液褪色③1 mol该物质最多能与4 mol H2加成④1 mol该物质最多能与含2 mol NaOH的溶液反应
A.①②③ B.①③④
C.③④ D.②③④
据悉,2012伦敦奥运会上使用的发令枪所用的“火药”成分是氯酸钾和红磷,经撞击发出响声,同时产生白色烟雾。撞击时发生的化学方程式为:
5KClO3+6P=3P2O5+5KCl,则下列有关叙述错误的是
| A.上述反应中氧化剂和还原剂的物质的量之比为5:6 |
| B.产生白色烟雾的原因是生成的P2 O5白色固体小颗粒(烟)吸水性很强,吸收空气中的水分,生成磷酸小液滴(雾) |
| C.上述反应中消耗3 mol P时,转移电子的物质的量为15mol |
| D.因红磷和白磷互为同素异形体,所以上述火药中的红磷可以用白磷代替 |