下列实验操作中正确的是
| A.蒸发结晶时应将溶液蒸干后再停止加热 |
| B.蒸馏操作时,应使温度计水银球插入蒸馏烧瓶的液体中 |
| C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D.用铂丝蘸取某溶液置于酒精灯火焰上灼烧,直接观察火焰颜色,检验K+的存在 |
乙酸橙花酯是一种食用香料,其结构简式如图,关于该有机物的叙述正确的是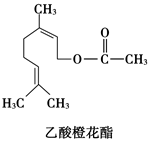
①属于芳香族化合物 ②不能发生银镜反应 ③分子式为C12H20O2
④不能使溴水褪色 ⑤1 mol该有机物水解时只能消耗1 mol NaOH
| A.②③⑤ | B.②③④ | C.①②③ | D.①④⑤ |
某有机化合物的结构简式为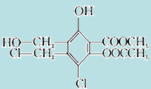
下列有关该物质的叙述正确的是
| A.1 mol该物质最多可以消耗3 mol Na |
| B.1 mol该物质最多可以消耗7 mol NaOH |
| C.不能与Na2CO3溶液反应 |
| D.易溶于水,可以发生加成反应和取代反应 |
1 mol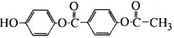 与足量的NaOH溶液充分反应,消耗的NaOH
与足量的NaOH溶液充分反应,消耗的NaOH
的物质的量为
| A.5 mol | B.4 mol | C.3 mol | D.2 mol |
下列关于有机化合物的认识不正确的是
| A.油脂在空气中完全燃烧转化为水和二氧化碳 |
| B.蔗糖、麦芽糖的分子式都是C12H22O11,二者互为同分异构体 |
| C.在水溶液里,乙酸分子中的—CH3可以电离出H+ |
| D.在浓硫酸存在下,苯与浓硝酸共热生成硝基苯的反应属于取代反应 |
下列关于有机物说法正确的是
| A.制乙酸乙酯时,把乙醇和乙酸依次加入浓硫酸中 |
| B.纤维素和淀粉都是多糖,二者互为同分异构体 |
| C.煤的干馏是物理变化,煤的气化和液化是化学变化 |
| D.三大合成材料是塑料、合成纤维和合成橡胶 |