如图,图Ⅰ表示10 mL量筒中液面的位置,A与B、B与C刻度间相差1 mL,图II表示50mL滴定管中液面的位置,D与E刻度间相差1 mL。如果刻度A和D都是4,则两处液面的读数是: ( )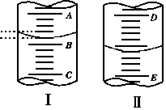
A.Ⅰ中是3.2 mL,Ⅱ中是3.40 mL
B.Ⅰ中是4.8 mL,Ⅱ中是3.40 mL
C.Ⅰ中是3.2 mL,Ⅱ中是4.60 mL
D.Ⅰ中是4.8 mL,Ⅱ中是4.60 mL
在pH为4~5的环境中,Cu2+、Fe2+不生成沉淀,而Fe3+几乎完全沉淀。工业上制CuCl2是将浓盐酸加热到80℃左右,再慢慢加入粗氧化铜(含杂质FeO),充分搅拌使之溶解。现欲除去溶液中的杂质离子,下述方法中可行的是()
| A.向溶液中加入纯Cu将Fe2+还原 |
| B.向溶液中通入H2S使Fe2+沉淀 |
| C.向溶液中通入Cl2,再通入CuO粉末调节pH为4~5 |
| D.向溶液中通入Cl2,再通入NH3调节pH为4~5 |
下列选项中所涉及到的两个量一定相等的是()
| A.36gH2O与1.204×1024个O2在标准状况下所占体积 |
| B.pH相等的氨水与醋酸溶液中由水电离出的OH-浓度 |
| C.pH相等的H2SO4和CH3COOH稀释相同倍数之后溶液的pH值 |
| D.等物质的量的Al分别与足量的盐酸、烧碱溶液反应转移的电子数 |
下列各组离子在指定条件下,一定能大量共存的是()
①能使红色石蕊试纸变蓝的溶液中:K+、Na+、CO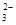 、
、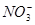 、[Al(OH)4]-
、[Al(OH)4]-
②c(H+)=10-1mol·L-1的溶液中:Cu2+、Al3+、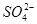
③能使碘化钾淀粉试纸变蓝的溶液中:Na+、NH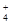 、S2-、Br-
、S2-、Br-
④水电离出的c(H)=10-13mol·L-1的溶液中:Na+、Mg2+、Cl-、SO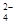
⑤在加入铝粉能产生H2的溶液中: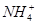 、Fe2+、SO
、Fe2+、SO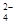 、NO
、NO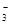
⑥在含大量Fe3+的溶液中:NH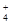 、Na+、Cl-、SCN-
、Na+、Cl-、SCN-
| A.①② | B.①③ |
| C.②④ | D.①②⑤⑥ |
下列说法正确的是()
| A.乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 |
| B.淀粉和纤维素都可作为工业上生产葡萄糖的原料 |
| C.用水可区分乙酸乙酯和苯 |
| D.钠跟乙醇反应比跟水反应剧烈 |
如右图所示,a、b是两根石墨棒,下列叙述不正确的是( )
| A.往滤纸上滴加酚酞试液,b极附近颜色变红 |
| B.a是正极,发生还原反应,b是负极,发生氧化反应 |
C.稀硫酸中硫酸 根离子的物质的量不变 根离子的物质的量不变 |
| D.装置工作时,稀硫酸溶液中C(H+)变小、C(Zn2+)变大 |