已知室温时,0.1 mol/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是( )
| A.该溶液的pH=4 |
B.升高温 度,溶液的pH增大 度,溶液的pH增大 |
| C.此酸的电离平衡常数约为1×10-7 |
| D.由HA电离出的c(H+)约为水电离出的c(H+)的106倍 |
短周期元素A、B、C的原子序数依次增大。已知:A、C同主族,而且三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半。下列叙述正确的是 ( )
A.原子半径:A<B<C
B.A单质的氧化性小于C单质
C.B的硫酸盐溶液pH<7
D.B元素单质可溶于酸但不溶于碱
依据元素周期律及元素周期表知识,下列推断正确的是 ( )
| A.酸性:H2SiO3>H2CO3 |
| B.热稳定性:H2Se>H2S>H2O |
| C.碱性:CsOH>Ca(OH)2 |
| D.若离子半径:R2->M+,则原子序数:R>M |
X、Y、Z为短周期元素,X原子最外层只有一个电子,Y原子的最外层电子数比内层电子总数少4,Z原子的最外层电子数是内层电子总数的三倍。下列有关叙述正确的是( )
| A.X、Y、Z三种元素可形成化合物X3YZ4 |
| B.X、Y两元素形成的化合物一定是离子化合物 |
| C.Y、Z两元素形成的化合物熔点较低 |
| D.稳定性:Y的氢化物>Z的氢化物 |
短周期元素甲、乙、丙、丁、戊五种元素在元素周期表中的位置如右图所示,其中戊是同周期中原子半径最小的元素。下列有关判断正确的是( )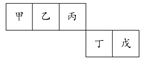
| A.最外层电子数:甲>乙>丙>丁>戊 |
| B.简单离子的离子半径:戊>丁 |
| C.含有丁元素的酸有多种 |
| D.乙的氢化物多种多样,丙、丁、戊的氢化物各有一种 |
下列说法中肯定错误的是( )
| A.某原子K层上只有一个电子 |
| B.某原子M层上电子数为L层上电子数的4倍 |
| C.某离子M层上和L层上的电子数均为K层的4倍 |
| D.某离子的核电荷数与最外层电子数相等 |