标准状况下,m g A气体与n g B气体分子数相等,下列说法不正确的是( )
| A.标准状况下,同体积的气体A和气体B的质量比为m∶n |
| B.25 ℃时,1 kg气体A与1 kg气体B的分子数之比为n∶m |
| C.标准状况下,等质量的A与B的体积比为m∶n |
| D.同温同压下,气体A与气体B的密度之比为m∶n |
下列说法中正确的是( )
| A.酯在一定条件下水解的产物一定是醇和酸 |
| B.完全燃烧某有机物,生成CO2和H2O的物质的量之比为1∶1,该有机物只可能是烯烃或环烷烃 |
| C.凡含有醛基的物质都能发生银镜反应,但不一定是醛类 |
| D.芳香烃的通式是CnH2n-6(n≥6) |
下列叙述不正确的是( )
| A.取淀粉和稀硫酸共热后的溶液,加入新制银氨溶液共热,没有银镜产生,证明淀粉尚未水解成葡萄糖 |
B.结构式为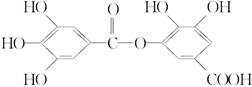 的有机物,可以在稀硫酸催化下发生水 的有机物,可以在稀硫酸催化下发生水解反应,但水解产物只有一种 |
| C.经唾液充分作用后的苹果中滴入碘水会显蓝色 |
| D.淀粉也是工业原料,可用于制葡萄糖和酒精 |
某高分子化合物干馏后分解为烃X,X能使溴水褪色,且1 mol X可与1 mol氢气加成后生成C8H10的烃,则该高分子化合物为()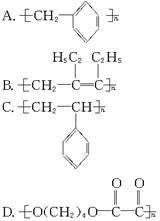
塑料制品废弃物会严重污染环境,常称为“白色污染”。为了防治这种污染,有一条重要途径是将合成高分子化合物重新变成小分子化合物,目前对结构为 的高分子化合物已成功实现这种处理,试分析若用CH3OH来处理它,能得到的有机物可能是()
的高分子化合物已成功实现这种处理,试分析若用CH3OH来处理它,能得到的有机物可能是()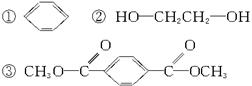
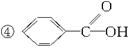
| A.①② | B.①③ | C.②③ | D.②④ |
以农副产品为原料可制得高分子材料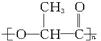 ,它能在乳酸菌作用下迅速降解,有希望用于制造一次性饭盒。有关该高分子的判断正确的是 ()
,它能在乳酸菌作用下迅速降解,有希望用于制造一次性饭盒。有关该高分子的判断正确的是 ()
| A.其相对分子质量一定是偶数 | B.其相对分子质量一定是奇数 |
| C.由其单体经加聚反应制得 | D.合成此高分子材料的单体有两种 |